题目内容
9. 对二甲苯(英文名称p-xylene,缩写为PX)是一种低毒化合物,也是聚酯工业的重要原料,主要用于生产对苯二甲酸(PTA),对苯二甲酸再和乙二醇(EG)反应生成聚对苯二甲酸乙二醇酯(PET).国内对二甲苯产量增长步伐放缓,供应缺口加大,近一半的PX依靠进口.以PX为主要原料生产PET的一种路线如图1:
对二甲苯(英文名称p-xylene,缩写为PX)是一种低毒化合物,也是聚酯工业的重要原料,主要用于生产对苯二甲酸(PTA),对苯二甲酸再和乙二醇(EG)反应生成聚对苯二甲酸乙二醇酯(PET).国内对二甲苯产量增长步伐放缓,供应缺口加大,近一半的PX依靠进口.以PX为主要原料生产PET的一种路线如图1:(1)PX可以发生的反应类型有加成反应、取代反应、氧化反应.(填反应类型)
(2)PX的核磁共振氢谱有2组峰,峰面积之比为2:3.
(3)反应②的化学方程式为
 .(不用注明条件)
.(不用注明条件)(4)PX的来源之一是煤的干馏.已知煤干馏副产物煤焦油主要成分有苯、甲苯、混合二甲苯、酚类等,从煤焦油中分离提纯对二甲苯的方法是分馏或蒸馏.
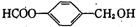
(5)“甲苯甲醇烷基化”制备对二甲苯是一条增产PX的新工艺路线(图2):写出该反应的化学方程式:
 .(不用注明条件)
.(不用注明条件)(6)PTA的一种同分异构体X与其含有相同官能团,且其苯环上的一氯取代物有两种,写出化合物X与1,3-丙二醇形成最简单环酯的结构简式:
 .
.
分析 (1)对二甲苯是苯的同系物,可发生取代反应,甲基可被氧化;
(2)根据对二甲苯的结构简式可判断核磁共振氢谱中峰的数目及峰面积之比;
(3)根据题中转化关系,对苯二甲酸与乙二醇发生缩聚反应生成聚对苯二甲酸乙二醇酯;
(4)煤焦油主要成分有苯、甲苯、混合二甲苯、酚类等,这些都是互溶的有机物,可利用它们沸点不同进行分离提纯;
(5)根据对二甲苯和甲苯的结构简式,利用元素守恒可写出图2中的化学方程式;
(6)对苯二甲酸中有两个羧基,X与其含有相同官能团,且其苯环上的一氯取代物有两种,说明两个相同的取代基位于苯环的邻位,则X为,X与1,3-丙二醇发生酯化反应形成最简单环酯,据此可写出其结构简式.
解答 解:(1)对二甲苯是苯的同系物,可发生取代反应,甲基可被氧化,发生氧化反应,
故答案为:取代反应;氧化反应;
(2)根据对二甲苯的结构简式可知,对二甲苯中有两种位置的氢原子,数目之比为4:6,所以核磁共振氢谱中峰的数目为2,峰面积之比为2:3,
故答案为:2;2:3;
(3)根据题中转化关系,对苯二甲酸与乙二醇发生缩聚反应生成聚对苯二甲酸乙二醇酯,反应的化学方程式为 ,
,
故答案为: ;
;
(4)煤焦油主要成分有苯、甲苯、混合二甲苯、酚类等,这些都是互溶的有机物,可利用它们沸点不同利用分馏或蒸馏的方法进行分离提纯,
故答案为:分馏或蒸馏;
(5)根据对二甲苯和甲苯的结构简式,利用元素守恒可写出图2中的化学方程式为 ,
,
故答案为: ;
;
(6)对苯二甲酸中有两个羧基,X与其含有相同官能团,且其苯环上的一氯取代物有两种,说明两个相同的取代基位于苯环的邻位,则X为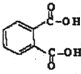 ,X与1,3-丙二醇发生酯化反应形成最简单环酯,其结构简式为
,X与1,3-丙二醇发生酯化反应形成最简单环酯,其结构简式为 ,
,
故答案为: .
.
点评 本题考查有机物推断与合成,是对有机化学基础的综合考查,需要学生熟练掌握官能团的性质与转化,难度中等.

 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案| A. | 单质的熔点、沸点高低 | |
| B. | 非金属之间发生的置换反应 | |
| C. | 非金属与氢气生成气态氢化物的难易程度 | |
| D. | 非金属元素的最高价氧化物的水化物的酸性强弱 |
| A. | sp-s | B. | sp2-s | C. | sp2-p | D. | sp3-s |
| A. | 22.4LH2 中含分子数为NA | |
| B. | 46gNO2 和N2O4混合气体中含有原子数为3NA | |
| C. | 1L1mol/L氨水溶液中离子总数为2NA | |
| D. | 1L2mol/L氯化铵溶液中有2NA个NH4+离子 |
(1)被还原的硫酸的物质的量为0.05mol.
(2)把反应后的溶液稀释至500ml,取出50ml,向其中加入足量的BaCl2溶液,得到沉淀20.27g,则稀释后所得溶液中SO42-的物质的量浓度为1.74mol/L(保留两位小数).
(3)若浓硫酸中含溶质为a mol,投入足量的铜片并加热,充分反应后,被还原的硫酸的物质的量n(H2SO4)<0.5amol.
(4)将产生的气体缓慢通入100ml b mol/L的氢氧化钠溶液中,若反应物均无剩余,则b的取值范围为0.5≤b≤1.
(5)讨论b的取值范围及与之对应的溶液的溶质及其物质的量,将结果填于下表中
| b的范围 | 溶质的种类 | 溶质的物质的量(mol) |
| 0.5 | NaHSO3 | 0.05 |
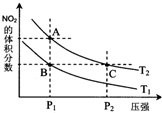 反应N2O4(g)?2NO2(g)△H=+57kJ•mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的是( )
反应N2O4(g)?2NO2(g)△H=+57kJ•mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的是( )| A. | A、C两点的反应速率:A>C | |
| B. | A、B两点气体的颜色:A浅,B深 | |
| C. | A、C两点气体的平均相对分子质量:A>C | |
| D. | 由状态B到状态A,可以用加热的方法 |
| A. | 先加入BaCl2溶液,再加入足量的HNO3溶液,产生了白色沉淀.溶液中一定含有大量的SO42- | |
| B. | 加入足量的CaCl2溶液,产生了白色沉淀.溶液中一定有大量的CO32- | |
| C. | 用洁净的铂丝蘸取该溶液,置于火焰上灼烧,透过蓝色钴玻璃能观察到火焰呈紫色.该溶液中一定含有钾离子,可能含有钠离子 | |
| D. | 先加适量的盐酸将溶液酸化,再加AgNO3溶液,产生了白色沉淀.溶液中一定含有大量的Cl- |
 平衡原理探究题
平衡原理探究题化学学科中存在着多种可逆过程和动态平衡,主要有化学平衡、电离平衡、水解平衡和沉淀溶解平衡等,且均遵循勒夏特列原理.请回答下列问题.
(1)一定温度下,在一个固定容积的密闭容器中,可逆反应
A(g)+2B(g)?4C(g)△H>0
达到平衡时,c(A)=2mol/L,c(B)=7mol/L,c(C)=4mol/L.试确定B的起始浓度c(B)的取值范围是[用c(B)、≤、≥、<、>、mol/L表示]3mol/L≤c(B)≤9mol/L,若改变条件重新达到平衡后体系中C的质量分数增大,下列措施可行的是C
A、增加C的物质的量 B、加压 C、升温 D、使用催化剂
(2)某学习小组探究盐样品K2CO3溶液显碱性的原因,取出少量向其中滴入2滴酚酞试液,溶液呈红色.甲同学认为是配制溶液所用样品中混有KOH,乙同学认为是盐水解.请你设计一个简单的实验方案给甲和乙两位同学的说法以评判,填空回答:
| 滴加试剂及量 | 所根据的现象 | 结论 |
| 是盐水解之故 |
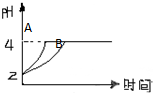
如图所示.则图中表示醋酸溶液中pH变化曲线的是B(填“A”或“B”).设盐酸中加入的Zn质量
为m1,醋酸溶液中加入的Zn质量为m2.则m1<m2(选填“<”、“=”、“>”)
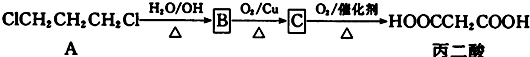

 .
.