12.下列含有共价键的离子化合物是( )
| A. | MgCl2 | B. | CO2 | C. | KOH | D. | 金刚石 |
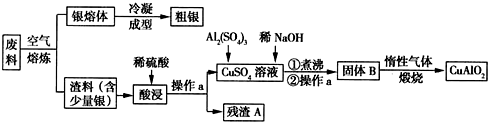
8.某工业含锰酸性废水的主要成分为MnSO4,另外还存在Fe2+、Fe3+、Al3+等离子.现以该废水为原料,制备高纯的碳酸锰,工业流程如下:
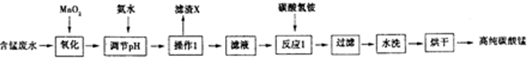
(1)加入MnO2的作用是MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O(用离子方程式表示).
(2)下表列出了几种离子生成氢氧化物沉淀时的pH
依据表中数据判断,用氨水调节溶液的pH应至5.2.
(3)滤渣X的主要成分为Fe(OH)3、Al(OH)3,滤液中的溶质为MnSO4、(NH4)2SO4.
(4)已知反应1中会产生一种气体,则该反应的化学方程式为2NH4HCO3+MnSO4=MnCO3+(NH4)2SO4+CO2↑+H2O.
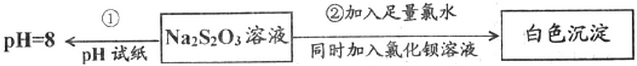
(5)判断水洗步骤中沉淀已洗净的方法是取最后一次的洗涤液于试管中,加入BaCl2溶液和稀硝酸,若无白色沉淀,说明已洗净.
(6)制得的碳酸锰可用于工业上电解法冶炼金属锰.该生产中需先将碳酸锰溶于强酸,配成电解液,写出该反应的离子方程式MnCO3+2H+=Mn2++CO2↑+H2O.

(1)加入MnO2的作用是MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O(用离子方程式表示).
(2)下表列出了几种离子生成氢氧化物沉淀时的pH
| 开始沉淀时的pH | 沉淀完全时的pH | |
| Fe3+ | 1.5 | 3.1 |
| Fe2+ | 6.5 | 9.7 |
| Al3+ | 3.3 | 5.2 |
| Mn2+ | 7.8 | 10.4 |
(3)滤渣X的主要成分为Fe(OH)3、Al(OH)3,滤液中的溶质为MnSO4、(NH4)2SO4.
(4)已知反应1中会产生一种气体,则该反应的化学方程式为2NH4HCO3+MnSO4=MnCO3+(NH4)2SO4+CO2↑+H2O.
(5)判断水洗步骤中沉淀已洗净的方法是取最后一次的洗涤液于试管中,加入BaCl2溶液和稀硝酸,若无白色沉淀,说明已洗净.
(6)制得的碳酸锰可用于工业上电解法冶炼金属锰.该生产中需先将碳酸锰溶于强酸,配成电解液,写出该反应的离子方程式MnCO3+2H+=Mn2++CO2↑+H2O.
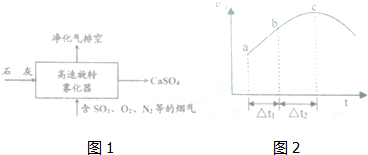
3.2014年全国各地都遭遇了“十面埋伏”,二氧化硫、氮氧化物和可吸入颗粒是雾霾的主要组成成分,综合治理其污染是环境化学当前的重要研究内容
(1)汽车尾气中的NO(g)和CO(g)在一定温度和催化剂的条件下可净化
①已知部分化学键的键能如下(键能指气态原子形成1mol化学键释放的最小能量)
汽车尾气进化中NO(g)和CO(g)发生反应的热化学方程式为2NO(g)+2CO(g)═N2(g)+2CO2(g)△H=-538kJ•mol-1
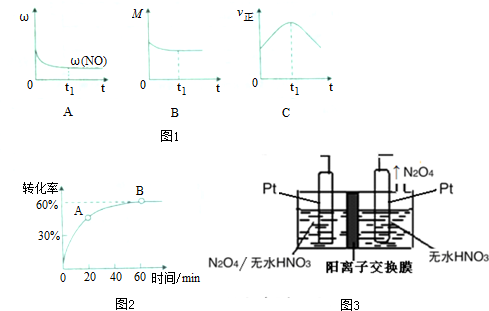
②若上述反应在绝热、恒荣的密闭体系中进行,并在t1时到达平衡状态,则下列示意图不符合题意的是C(填选项序号)(图中1ω、M、?、z分别表示质量分数、混合气体平均相对分子质量、正反应速率)
(2)尾气中的SO2可先催化氧化生成SO2,再合成硫酸,已知:
2SO${\;}_{{\;}_{2}}$(g)+O2(g)$?_{高温}^{催化剂}$2SO2(g)△H=-196.0kj/mol
①在一定温度的密闭容器中,SO2的转化率时间的变化关系如图2所示,则A点的正反应速率v正(SO2)<B点的正反应速率v正(SO2)(填“大于”、“小于”或“等于”)
②在某温度时,向10L的密闭容器中加入4.0mol SO2和10.0mol O2,反应达到平衡,改变下列条件,再次达到平衡时,能使O2的新平面浓度和原来平衡浓度相同的是BC(填选项序号)
A.在其他条件不变时,减少容器的容积
B.保持温度和容器内压强不变,再充入2.0mol SO2和5.0mol O2
C.保持温度和容器体积不变,再充入SO2和SO3,使之浓度扩大为原来的两倍
(3)用NH3催化还原NO2也可以消除氮氧化物的污染,反应原理为:
NO(g)+NO2(g)+2NH3(g)?2N2(g)+3H2O(g)
对于气体反应,用某组分(B)的平衡压强(pB)代替物质的量浓度(cb)也可以表示平衡常数(记作Kp),则上述反应的K的表达式为$\frac{{p}^{3}({H}_{2}O){p}^{2}({N}_{2})}{p(NO)p(N{O}_{2}){p}^{2}(N{H}_{3})}$
(4)以N2O4为原料采用电解法可制备新型绿色硝化剂N2O3,实验装置如图3所示,电解池中生成N2O3的电极反应式为N2O4+2HNO3-e-=2N2O3+O2↑+2H+
(5)尾气中氢氧化物(NO和NO2)可用尿素[CO(NH2)3]溶液除去,反应生成对大气无污染的气体,1mol尿素能吸收工业尾气中氢氧化物(假设NO、NO2体积比为1:1)的质量为76g.
0 168895 168903 168909 168913 168919 168921 168925 168931 168933 168939 168945 168949 168951 168955 168961 168963 168969 168973 168975 168979 168981 168985 168987 168989 168990 168991 168993 168994 168995 168997 168999 169003 169005 169009 169011 169015 169021 169023 169029 169033 169035 169039 169045 169051 169053 169059 169063 169065 169071 169075 169081 169089 203614
(1)汽车尾气中的NO(g)和CO(g)在一定温度和催化剂的条件下可净化
①已知部分化学键的键能如下(键能指气态原子形成1mol化学键释放的最小能量)
| 化学键 | N=O | C≡O | C=O | N≡N |
| 键能(kj/mol) | 632 | 1072 | 750 | 946 |
②若上述反应在绝热、恒荣的密闭体系中进行,并在t1时到达平衡状态,则下列示意图不符合题意的是C(填选项序号)(图中1ω、M、?、z分别表示质量分数、混合气体平均相对分子质量、正反应速率)
(2)尾气中的SO2可先催化氧化生成SO2,再合成硫酸,已知:
2SO${\;}_{{\;}_{2}}$(g)+O2(g)$?_{高温}^{催化剂}$2SO2(g)△H=-196.0kj/mol
①在一定温度的密闭容器中,SO2的转化率时间的变化关系如图2所示,则A点的正反应速率v正(SO2)<B点的正反应速率v正(SO2)(填“大于”、“小于”或“等于”)
②在某温度时,向10L的密闭容器中加入4.0mol SO2和10.0mol O2,反应达到平衡,改变下列条件,再次达到平衡时,能使O2的新平面浓度和原来平衡浓度相同的是BC(填选项序号)
A.在其他条件不变时,减少容器的容积
B.保持温度和容器内压强不变,再充入2.0mol SO2和5.0mol O2
C.保持温度和容器体积不变,再充入SO2和SO3,使之浓度扩大为原来的两倍
(3)用NH3催化还原NO2也可以消除氮氧化物的污染,反应原理为:
NO(g)+NO2(g)+2NH3(g)?2N2(g)+3H2O(g)
对于气体反应,用某组分(B)的平衡压强(pB)代替物质的量浓度(cb)也可以表示平衡常数(记作Kp),则上述反应的K的表达式为$\frac{{p}^{3}({H}_{2}O){p}^{2}({N}_{2})}{p(NO)p(N{O}_{2}){p}^{2}(N{H}_{3})}$
(4)以N2O4为原料采用电解法可制备新型绿色硝化剂N2O3,实验装置如图3所示,电解池中生成N2O3的电极反应式为N2O4+2HNO3-e-=2N2O3+O2↑+2H+
(5)尾气中氢氧化物(NO和NO2)可用尿素[CO(NH2)3]溶液除去,反应生成对大气无污染的气体,1mol尿素能吸收工业尾气中氢氧化物(假设NO、NO2体积比为1:1)的质量为76g.


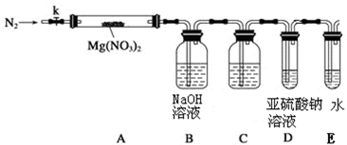 某学习小组以Mg(NO3)2为研究对象,拟通过实验初步探究硝酸盐热分解的规律.
某学习小组以Mg(NO3)2为研究对象,拟通过实验初步探究硝酸盐热分解的规律. 乳酸亚铁晶体([CH3CH(OH)COO]2Fe•3H2O,Mr=288)是常用的补铁剂.乳酸亚铁可由乳酸与碳酸亚铁(易被空气中氧气氧化)反应制得:2CH3CH(OH)COOH+FeCO3→[CH3CH(OH)COO]2Fe+CO2↑+H2O.
乳酸亚铁晶体([CH3CH(OH)COO]2Fe•3H2O,Mr=288)是常用的补铁剂.乳酸亚铁可由乳酸与碳酸亚铁(易被空气中氧气氧化)反应制得:2CH3CH(OH)COOH+FeCO3→[CH3CH(OH)COO]2Fe+CO2↑+H2O.