10.关于平衡常数,下列说法不正确的是( )
| A. | 平衡常数不随反应物或生成物的浓度的改变而改变 | |
| B. | 平衡常数随温度的改变而改变 | |
| C. | K值越大,反应进行的程度越大 | |
| D. | 温度越高,K值越大 |
9.在一定条件下,反应CO+NO2?CO2+NO,达到平衡后,降低温度,混和气体的颜色变浅.下列判断正确的是( )
| A. | 正反应为吸热反应 | B. | 正反应为放热反应 | ||
| C. | CO的平衡转化率降低 | D. | 各物质的浓度不变 |
8.有关如图装置的叙述不正确的是( )


| A. | 这是电解NaOH溶液的装置 | |
| B. | 该装置中Pt为正极,电极反应为O2+2H2O+4e-→4OH- | |
| C. | 该装置中Fe为负极,电极反应为Fe+2OH-→Fe(OH)2+2e- | |
| D. | 这是一个原电池装置 |
7.下面有关电化学的图示,完全正确的是( )
| A. | 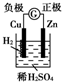 Cu-Zn原电池 | B. | 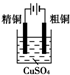 粗铜的精炼 | ||
| C. | 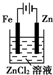 铁片镀锌 | D. | 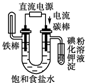 验证NnCl溶液(含酚酞) |
6.下列说法正确的是( )
| A. | 书写热化学方程式时,只要在化学方程式的右端写上热量的符号和数值即可 | |
| B. | 凡是在加热或点燃条件下进行的反应都是吸热反应 | |
| C. | 把化学反应中物质的变化和反应的焓变同时表示出的化学方程式叫做热化学方程式 | |
| D. | 氢气在氧气中燃烧的热化学方程式是2H2(g)+O2(g)═2H2O(l)△H=-571.6 kJ |
5.已知Zn(s)+H2SO4(aq)═ZnSO4(aq)+H2(g)△H<0,则下列关于该反应的叙述不正确的是( )
| A. | 该反应中旧键断裂需要吸收能量,新键形成需放出能量,所以总能量不变 | |
| B. | 上述热化学方程式中的△H的值与反应物的用量无关 | |
| C. | 该反应为放热反应 | |
| D. | 反应物的总能量高于生成物的总能量 |
4.只用一种试剂就可将AgNO3、KSCN和H2SO4、NaOH四种无色溶液区分,这种试剂是( )
| A. | Fe(NO3)3溶液 | B. | FeCl2溶液 | C. | BaCl2溶液 | D. | FeCl3溶液 |
2.含n g硝酸的稀溶液恰好和m g铁粉完全反应若有$\frac{n}{4}$g HNO3 被还原成NO,n:m可能( )
| A. | 1:1 | B. | 2:1 | C. | 3:1 | D. | 9:2 |
1.设阿伏加德罗常数为NA,则下列说法正确的是( )
0 168470 168478 168484 168488 168494 168496 168500 168506 168508 168514 168520 168524 168526 168530 168536 168538 168544 168548 168550 168554 168556 168560 168562 168564 168565 168566 168568 168569 168570 168572 168574 168578 168580 168584 168586 168590 168596 168598 168604 168608 168610 168614 168620 168626 168628 168634 168638 168640 168646 168650 168656 168664 203614
| A. | 1.5g甲基(-CH3)所含有的电子数是NA | |
| B. | 14g乙烯和丙烯的混合物中含有原子的数目为NA | |
| C. | 标准状况下,1 L戊烷充分燃烧后生成的气态产物的分子数为$\frac{5}{22.4}$NA | |
| D. | 常温常压下,1mol CnH2n+2中所含有的共价键数目为(3n+1)NA |