题目内容
7.下面有关电化学的图示,完全正确的是( )| A. | 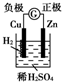 Cu-Zn原电池 | B. | 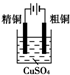 粗铜的精炼 | ||
| C. | 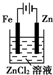 铁片镀锌 | D. | 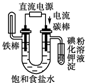 验证NnCl溶液(含酚酞) |
分析 A、依据原电池原理分析,活泼金属做负极;
B、粗铜精炼,粗铜做阳极,精铜做阴极;
C、依据电镀原理,镀层金属做阳极,待镀金属做阴极;
D、电解饱和食盐水,铁棒为阴极,电解过程中生成氢气,碳棒做电解池阳极,溶液中氯离子失电子生成氯气.
解答 解:A、依据原电池原理分析,活泼金属锌做负极,铜做正极,故A错误;
B、粗铜精炼,粗铜做阳极,精铜做阴极,故B错误;
C、镀件铁做阴极,铜做阳极进行电镀,故C错误;
D、电解饱和食盐水,阳极电流流向,铁棒为阴极,电解过程中生成氢气,碳棒做电解池阳极,溶液中氯离子失电子生成氯气,检验氯气用淀粉碘化钾,故D正确;
故选D.
点评 本题考查了原电池和电解池原理的分析判断,电极反应和电极判断是解题关键,题目难度中等.

练习册系列答案
相关题目
17.不能用磨口玻璃瓶贮存的一组物质是( )
| A. | 盐酸、硫酸、Fe2(SO4)3溶液 | B. | NaCl、KCl、AgNO3溶液 | ||
| C. | NaOH溶液、水玻璃 | D. | MnO2、KClO3、KMnO4固体 |
15.下列各组物质中,互为同位素的是( )
| A. | 重氢、超重氢 | B. | 氧、臭氧 | C. | 红磷、白磷 | D. | 乙酸、丙酸 |
2.含n g硝酸的稀溶液恰好和m g铁粉完全反应若有$\frac{n}{4}$g HNO3 被还原成NO,n:m可能( )
| A. | 1:1 | B. | 2:1 | C. | 3:1 | D. | 9:2 |
12.在注射器内充入NO2,平衡后在恒温下进行压缩,当体积减小$\frac{1}{4}$时,则( )
| A. | 体系颜色比原来深 | B. | 体系颜色比原来浅 | ||
| C. | 体系颜色不变 | D. | 注射器内压强不变 |
19.常温下,某氨水的pH=x,某盐酸的pH=Y,已知x+y=14,将上述氨水与盐酸等体积混合后,所得溶液中各种离子浓度的关系正确的是( )
| A. | c(Cl-)>c(NH4+)>c(H+)>c(OH-) | B. | c(Cl-)>c( NH4+)>c(OH-)>c(H+) | ||
| C. | c( NH4+)>c(Cl-)>c(OH-)>c(H+) | D. | c( NH4+)+c(NH3.H2O)=c(Cl-) |
16.下列说法正确的是( )
| A. | 青铜是我国使用最早的合金,也是目前使用最广泛的合金 | |
| B. | 不管哪种铜合金都含有铜元素,所以它们的性质也和金属铜一样 | |
| C. | 我们日常生活中用到的铜合金制品主要是黄铜制的 | |
| D. | 各种铜合金都有良好的导电、导热性 |
17.下列制备和收集气体的实验装置合理的是( )
| A. |  用氯化铵和氢氧化钙制NH3 | B. |  二氧化锰和浓盐酸制氯气 | ||
| C. |  用锌粒和稀硫酸制H2 | D. |  用双氧水和二氧化锰制O2 |