10.下列关于材料的说法,正确的是( )
| A. | 铝具有很强的抗腐蚀能力,是因为其不易与氧气发生反应 | |
| B. | 棉布,羊毛和绦纶燃烧后都生成二氧化碳和水 | |
| C. | 航天飞机上的陶瓷防护片属于新型无机非金属材料 | |
| D. | 食品保鮮膜、塑料水杯等生活用品的主要成分是聚氯乙烯 |
9.氮及其化合物在工农业生产、生活中有重要作用.请按要求回答下列相关问题:
(1)食品添加剂铵明矾NH4Al(SO4)2•12H2O高温可分解,下列关于其分解产物的预测不合理的是C
A.NH3、N2、SO2、H2O
B.NH3、SO3、H2O
C.NH3、SO2、H2O
D.NH3、N2、SO3、SO2、H2O
(2)汽车发动机工作时也会引发N2和O2反应产生大气污染物NO,其能量变化示意图为图1: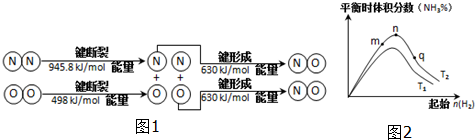
该反应的热化学方程式为N2(g)+O2(g)=2NO(g)△H=+183.8kJ/mol.
(3)工业合成氨的反应:N2(g)+3H2(g)?2NH3(g)△H<0,分别在T1、T2温度下,改变起始氢气物质的量,测得平衡时氨的体积分数如图2示:
①比较在m、n、q三点所处的平衡状态中,反应物N2的转化率最高的是p点.
②T2条件下,在2L的密闭容器中,充入x mol N2和y mol H2时,3min达平衡,此时反应物的转化率均为a,
写出下列仅含a、x的表达式(不必化简):
v(N2)=$\frac{xa}{6}$mol•L-1•min-1;该反应的平衡常数的值K=$\frac{16(xa)^{2}}{(x-xa)(3x-3xa)^{3}}$.
③图象中T2低于T1(填“高于”、“低于”、“等于”或“无法确定”).
④科学家采用高质子导电性的SCY陶瓷(能传递H+ )实现氨的电化学合成,这提高了氮气和氢气的转化率.写出电化学合成过程中发生还原反应的电极方程式:N2+6H++6e-=2NH3.
(4)将质量相等的四份铁粉和铜粉的均匀混合物,分别加入同浓度稀硝酸充分反应,(假设硝酸的还原产物只有NO)实验数据如下表:
下列有关分析推断正确的是AC.
A.硝酸起始浓度为4mol/L
B.①中溶解了5.6g Fe
C.③中n(Cu2+)=0.15mol
D.④中V=6.72L.
(1)食品添加剂铵明矾NH4Al(SO4)2•12H2O高温可分解,下列关于其分解产物的预测不合理的是C
A.NH3、N2、SO2、H2O
B.NH3、SO3、H2O
C.NH3、SO2、H2O
D.NH3、N2、SO3、SO2、H2O
(2)汽车发动机工作时也会引发N2和O2反应产生大气污染物NO,其能量变化示意图为图1:

该反应的热化学方程式为N2(g)+O2(g)=2NO(g)△H=+183.8kJ/mol.
(3)工业合成氨的反应:N2(g)+3H2(g)?2NH3(g)△H<0,分别在T1、T2温度下,改变起始氢气物质的量,测得平衡时氨的体积分数如图2示:
①比较在m、n、q三点所处的平衡状态中,反应物N2的转化率最高的是p点.
②T2条件下,在2L的密闭容器中,充入x mol N2和y mol H2时,3min达平衡,此时反应物的转化率均为a,
写出下列仅含a、x的表达式(不必化简):
v(N2)=$\frac{xa}{6}$mol•L-1•min-1;该反应的平衡常数的值K=$\frac{16(xa)^{2}}{(x-xa)(3x-3xa)^{3}}$.
③图象中T2低于T1(填“高于”、“低于”、“等于”或“无法确定”).
④科学家采用高质子导电性的SCY陶瓷(能传递H+ )实现氨的电化学合成,这提高了氮气和氢气的转化率.写出电化学合成过程中发生还原反应的电极方程式:N2+6H++6e-=2NH3.
(4)将质量相等的四份铁粉和铜粉的均匀混合物,分别加入同浓度稀硝酸充分反应,(假设硝酸的还原产物只有NO)实验数据如下表:
| 编 号 | ① | ② | ③ | ④ |
| 稀硝酸体积/mL | 100mL | 200mL | 300mL | 400mL |
| 剩余金属/g | 18.0g | 9.6g | 0 | 0 |
| NO体积/L(标准状况下) | 2.24L | 4.48L | 6.72L | V |
A.硝酸起始浓度为4mol/L
B.①中溶解了5.6g Fe
C.③中n(Cu2+)=0.15mol
D.④中V=6.72L.
8.下列排列顺序错误的是( )
| A. | 键能:C≡C>C=C>C-C | B. | 键长:C-C>C=C>C≡C | ||
| C. | 沸点:C5H8>C4H6>C3H4 | D. | 分子活性:C2H6>C2H4>C2H2 |
6.当前我国环境状况不荣乐观,其中PM2.5、CO、SO2、NOx等污染物对空气质量的影响非常显著,其主要来源为燃煤、机动车尾气等,因此,对其进行研究具有重要意义,请回答下列问题:
(1)对某地PM2.5样本用蒸馏水处理后,测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
根据表中数据计算该试样的pH=4.
(2)NOx是汽车尾气的主要污染物之一.汽车发动机工作时会引发N2和O2反应,其能量变化示意图1如下:
①写出N2和O2反应的热化学方程式N2(g)+O2(g)=2NO(g)△H=-120kJ•mol-1.
②处理尾气时,加装催化转化装置使NOx与CO转变为无污染的气体排放,请写出该反应的化学方程式2NOx+2xCO$\frac{\underline{\;催化剂\;}}{\;}$N2+2xCO2
③有人设想将CO按下列反应除去:2CO(g)=2C(s)+O2(g)△H>0,请你分析该设想能否实现?不能(填“是”或“否”),依据是该反应是焓增、熵减的反应,根据G=△H-T•△S,G>0.
④另有人认为以如图2所示原电池原理也可以除去CO,则其正极反应式为O2+2CO2+4e-=2CO32-.容器中的CO32-离子A极移动(填“A”或“B”).
(3)利用I2O5消除CO污染的反应为:5CO(g)+I2O5(s)?5CO2(g)+I2(s),不同温度下,向装有足量I2O5固体的2L恒容密闭容器中通入2mol CO,测得CO2的体积分数随时间t变化曲线如图3.请回答下列问题:
①T1时化学平衡常数K=1024
②下列说法正确的是AD(填字母序号).
A.容器内气体密度不变,表明反应达到平衡状态
B.该反应的△H>0
C.d点时,向恒容容器中充入2molCO,再次平衡后,CO2的含量增大.
D.T1与T2化学平衡常数大小关系:K(T1)>K(T2)
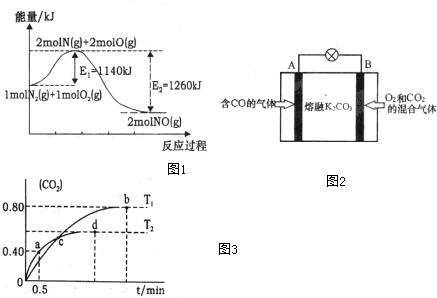
(1)对某地PM2.5样本用蒸馏水处理后,测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
| 离子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 浓度/mol•L-1 | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
(2)NOx是汽车尾气的主要污染物之一.汽车发动机工作时会引发N2和O2反应,其能量变化示意图1如下:
①写出N2和O2反应的热化学方程式N2(g)+O2(g)=2NO(g)△H=-120kJ•mol-1.
②处理尾气时,加装催化转化装置使NOx与CO转变为无污染的气体排放,请写出该反应的化学方程式2NOx+2xCO$\frac{\underline{\;催化剂\;}}{\;}$N2+2xCO2
③有人设想将CO按下列反应除去:2CO(g)=2C(s)+O2(g)△H>0,请你分析该设想能否实现?不能(填“是”或“否”),依据是该反应是焓增、熵减的反应,根据G=△H-T•△S,G>0.
④另有人认为以如图2所示原电池原理也可以除去CO,则其正极反应式为O2+2CO2+4e-=2CO32-.容器中的CO32-离子A极移动(填“A”或“B”).
(3)利用I2O5消除CO污染的反应为:5CO(g)+I2O5(s)?5CO2(g)+I2(s),不同温度下,向装有足量I2O5固体的2L恒容密闭容器中通入2mol CO,测得CO2的体积分数随时间t变化曲线如图3.请回答下列问题:
①T1时化学平衡常数K=1024
②下列说法正确的是AD(填字母序号).
A.容器内气体密度不变,表明反应达到平衡状态
B.该反应的△H>0
C.d点时,向恒容容器中充入2molCO,再次平衡后,CO2的含量增大.
D.T1与T2化学平衡常数大小关系:K(T1)>K(T2)

5.硼和铝是同主族元素,在生产、生活和科研中具有广泛的应用.以下是几种常见的硼化合物:
请回答下列问题:
(1)写出硼元素在周期表中的位置第二周期ⅢA族.
(2)工业上以硼镁矿为原料制取硼,该工艺的中间过程会发生反应:B2O3+3Mg=2B+3MgO,则每生成1mol的硼转移的电子数为3NA.
(3)工业上常用金属铝冶炼难熔金属,请写出以五氧化二矾(V2O5)和铝为原料获得金属矾的化学方程式3V2O5+10Al$\frac{\underline{\;高温\;}}{\;}$6V+5Al2O3.
(4)硼酸是一种一元弱酸,它与水作用时结合水电离的OH-而释放出水电离的H+,皮肤上不小心碰到氢氧化钠溶液,一般先用大量水冲洗,然后再涂上硼酸溶液,请写出硼酸与氢氧化钠反应的离子方程式H3BO3+OH-=[B(OH)4]-.
(5)硼氢化钠(NaBH4)是一种强还原剂,遇水剧烈反应产生大量气体,请写出该反应的化学方程式NaBH4+2H2O═NaBO2+4H2↑.
(6)偏硼酸钠能溶于水,其溶液显碱性(填“酸性”、“中性”或“碱性”),原因是BO2-+2H2O?H3BO3+OH-(用离子方程式表示)
| 硼镁矿 | 硼砂 | 硼酸 | 偏硼酸钠 |
| Mg2B2O5•H2O | Na2B4O7•10H2O | H3BO3 | NaBO2 |
(1)写出硼元素在周期表中的位置第二周期ⅢA族.
(2)工业上以硼镁矿为原料制取硼,该工艺的中间过程会发生反应:B2O3+3Mg=2B+3MgO,则每生成1mol的硼转移的电子数为3NA.
(3)工业上常用金属铝冶炼难熔金属,请写出以五氧化二矾(V2O5)和铝为原料获得金属矾的化学方程式3V2O5+10Al$\frac{\underline{\;高温\;}}{\;}$6V+5Al2O3.
(4)硼酸是一种一元弱酸,它与水作用时结合水电离的OH-而释放出水电离的H+,皮肤上不小心碰到氢氧化钠溶液,一般先用大量水冲洗,然后再涂上硼酸溶液,请写出硼酸与氢氧化钠反应的离子方程式H3BO3+OH-=[B(OH)4]-.
(5)硼氢化钠(NaBH4)是一种强还原剂,遇水剧烈反应产生大量气体,请写出该反应的化学方程式NaBH4+2H2O═NaBO2+4H2↑.
(6)偏硼酸钠能溶于水,其溶液显碱性(填“酸性”、“中性”或“碱性”),原因是BO2-+2H2O?H3BO3+OH-(用离子方程式表示)
4.已知2-丁烯有顺、反两种异构体,在某条件下两种气体处于平衡,下列说法正确的是( )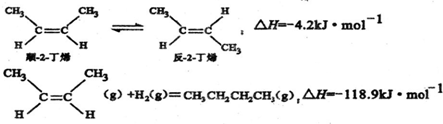

| A. | 反-2-丁烯比顺-2-丁烯稳定 | |
| B. | 顺-2-丁烯的燃烧热数值比反-2-丁烯小 | |
| C. | 减压和升温有利于平衡向生成正丁烷反应方向移动 | |
| D. | 反-2-丁烯氢化的热化学方程式为: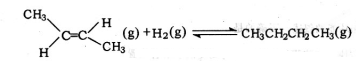 △H=-123.1kJ•mol-1 △H=-123.1kJ•mol-1 |
3.设阿伏伽德罗常数为NA,下列说法正确的是( )
| A. | 6.4g由S2、S4、S8组成的混合物中所含硫原子数为0.2NA | |
| B. | 用100ml 4mol/L盐酸与8.7g MnO2供热能制取氯气4.48L | |
| C. | 一定温度下,0.1L 0.1mol/L的CH3COOH溶液和1L 0.01mol/L 的CH3COOH溶液所含CH3COO-的数目均为0.01NA | |
| D. | 一定条件下,将1mol N2和3 mol H2混合,充分反应后转移的电子数为6 NA |
2.从化学角度分析,下列叙述不正确的是( )
0 167879 167887 167893 167897 167903 167905 167909 167915 167917 167923 167929 167933 167935 167939 167945 167947 167953 167957 167959 167963 167965 167969 167971 167973 167974 167975 167977 167978 167979 167981 167983 167987 167989 167993 167995 167999 168005 168007 168013 168017 168019 168023 168029 168035 168037 168043 168047 168049 168055 168059 168065 168073 203614
| A. | 银氨溶液或新制Cu(OH)2均能检验糖尿病人尿液中的葡萄糖 | |
| B. | 在燃煤中加入适量生石灰,可以减少二氧化硫的排放 | |
| C. | 铜制品在潮湿环境中的腐蚀比干燥环境中快 | |
| D. | 生活中的水杯、奶瓶、食物保鲜膜等可以使用聚氯乙烯来制造 |

 .
. 