6.同周期的X.Y.Z三种元素,已知它们的最高价氧化物对应的水化物是HXO4、H2YO4、H3ZO4,则下列判断正确的是( )
| A. | 含氧酸的酸性:H3ZO4>H2YO4>HXO4 | |
| B. | 非金属性:X>Y>Z | |
| C. | 气态氢化物的稳定性按X、Y、Z顺序由弱到强 | |
| D. | 元素的负化合价的绝对值按X、Y、Z顺序由大到小 |
5.下列电子式正确的是( )
| A. | H2O2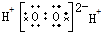 | B. | HClO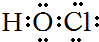 | C. | MgCl2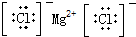 | D. | CCl4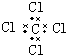 |
4.如图是某有机物的质谱图,其相对分子质量为( )
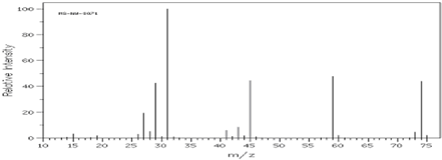

| A. | 74 | B. | 31 | C. | 59 | D. | 45 |
3.一种氢氧燃料电池的电解液为KOH溶液.下列有关该电池的叙述不正确的是( )
| A. | 正极反应式为:O2+2H2O+4e-═4OH- | |
| B. | 工作一段时间后,电解液中KOH的物质的量不变 | |
| C. | 该燃料电池的总反应方程式为:2H2+O2═2H2O | |
| D. | H2通入的一极为正极 |
2.化合物X2Y由短周期元素X和Y组成.下列说法一定正确的是( )
| A. | X的原子半径大于Y | |
| B. | 若X为ⅠA族元素,则该化合物中含离子键 | |
| C. | 若X2Y的焰色为黄色,则它的电子式是 | |
| D. | 若每个X2Y分子中含有10个电子,则Y是第3周期元素 |
1.用水稀释0.1mol L-1的醋酸溶液,其中随水的增加而增大的有( )
①H+的物质的量,②c(H+),③c(OH-),④$\frac{c({H}^{+})}{c(HAc)}$,⑤$\frac{c(HAc)}{c(A{c}^{-})}$.
①H+的物质的量,②c(H+),③c(OH-),④$\frac{c({H}^{+})}{c(HAc)}$,⑤$\frac{c(HAc)}{c(A{c}^{-})}$.
| A. | ①③④ | B. | ①③⑤ | C. | ②④ | D. | ③④ |
20.某无色溶液加入铝可以生成氢气,则在该溶液中可能大量存在的离子组是( )
| A. | K+、NH4+、NO3-、Cl- | B. | Na+、K+、NH4+、Cl- | ||
| C. | NH4+、K+、HCO3-、Cl- | D. | Na+、Cu2+、Br-、Cl- |
19.已知:I2+2S2O32-═S4O62-+2I-,相关物质的溶度积常数见下表:
(1)常温下,某酸性CuCl2溶液中含有少量的FeCl3,为得到纯净的CuCl2•2H2O晶体,加入Cu(OH)2、CuO、CuCO3或Cu2(OH)2CO3,调至pH=4,使溶液中的Fe3+转化为Fe(OH)3沉淀,此时溶液中的c(Fe3+)=2.6×10-9mol/L.过滤后,将所得滤液低温蒸发、浓缩结晶,可得到CuCl2•2H2O晶体.
(2)在空气中直接加热CuCl2•2H2O晶体得不到纯的无水CuCl2,而是生成Cu(OH)Cl,写出相关的化学反应方程式:CuCl2•2H2O$\frac{\underline{\;\;△\;\;}}{\;}$Cu(OH)Cl+HCl↑+H2O.由CuCl2•2H2O晶体得到纯的无水CuCl2的合理方法是在干燥HCl气流中加热制得.
(3)某学习小组用“间接碘量法”测定含有CuCl2•2H2O晶体的试样(不含能与I-发生反应的氧化性杂质)的纯度,过程如下:取0.36g试样溶于水,加入过量KI固体,充分反应,生成白色CuI沉淀.过滤后,用0.100 0mol•L-1 Na2S2O3标准溶液滴定所得滤液,到达滴定终点时,消耗Na2S2O3标准溶液20.00mL.
①可选用淀粉作滴定指示剂,滴定终点的现象是蓝色变为无色,且在半分钟内无变化.
②CuCl2溶液与KI反应的离子方程式为2Cu2++4I-=2CuI↓+I2.
③该试样中CuCl2•2H2O的质量百分数为95.0%.
0 167731 167739 167745 167749 167755 167757 167761 167767 167769 167775 167781 167785 167787 167791 167797 167799 167805 167809 167811 167815 167817 167821 167823 167825 167826 167827 167829 167830 167831 167833 167835 167839 167841 167845 167847 167851 167857 167859 167865 167869 167871 167875 167881 167887 167889 167895 167899 167901 167907 167911 167917 167925 203614
| 物质 | Cu(OH)2 | Fe(OH)3 | CuCl | CuI |
| Ksp | 2.2×10-20 | 2.6×10-39 | 1.7×10-7 | 1.3×10-12 |
(2)在空气中直接加热CuCl2•2H2O晶体得不到纯的无水CuCl2,而是生成Cu(OH)Cl,写出相关的化学反应方程式:CuCl2•2H2O$\frac{\underline{\;\;△\;\;}}{\;}$Cu(OH)Cl+HCl↑+H2O.由CuCl2•2H2O晶体得到纯的无水CuCl2的合理方法是在干燥HCl气流中加热制得.
(3)某学习小组用“间接碘量法”测定含有CuCl2•2H2O晶体的试样(不含能与I-发生反应的氧化性杂质)的纯度,过程如下:取0.36g试样溶于水,加入过量KI固体,充分反应,生成白色CuI沉淀.过滤后,用0.100 0mol•L-1 Na2S2O3标准溶液滴定所得滤液,到达滴定终点时,消耗Na2S2O3标准溶液20.00mL.
①可选用淀粉作滴定指示剂,滴定终点的现象是蓝色变为无色,且在半分钟内无变化.
②CuCl2溶液与KI反应的离子方程式为2Cu2++4I-=2CuI↓+I2.
③该试样中CuCl2•2H2O的质量百分数为95.0%.
 ⑧
⑧