题目内容
4.如图是某有机物的质谱图,其相对分子质量为( )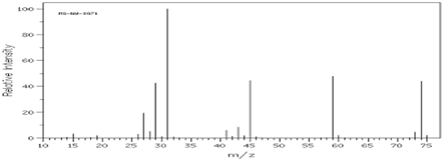
| A. | 74 | B. | 31 | C. | 59 | D. | 45 |
分析 根据质谱图中最右边的那个峰就是该物质的相对分子质量.
解答 解:根据质谱图中最右边的那个峰就是该物质的相对分子质量,根据质谱图可知,该有机物的相对分子质量为74,
故选A.
点评 本题考查了有机物分子式的确定,题目难度中等,明确质谱图的含义,能够根据质谱图判断物质的相对分子量.

练习册系列答案
 特高级教师点拨系列答案
特高级教师点拨系列答案
相关题目
15.下列说法中,正确的是( )
| A. | 任何溶液中,c(H+)×c(OH-)=1.0×10-14 | |
| B. | pH=0的溶液呈中性 | |
| C. | 酸性溶液中,c(H+)越大,酸性越强 | |
| D. | 酸性溶液中没有OH-,碱性溶液里没有H+ |
12.某元素原子的N层上只有1或2个电子,则该原子的M层上的电子数可能为( )
| A. | 8 | B. | 18 | C. | 8~18 | D. | 18~32 |
19.已知:I2+2S2O32-═S4O62-+2I-,相关物质的溶度积常数见下表:
(1)常温下,某酸性CuCl2溶液中含有少量的FeCl3,为得到纯净的CuCl2•2H2O晶体,加入Cu(OH)2、CuO、CuCO3或Cu2(OH)2CO3,调至pH=4,使溶液中的Fe3+转化为Fe(OH)3沉淀,此时溶液中的c(Fe3+)=2.6×10-9mol/L.过滤后,将所得滤液低温蒸发、浓缩结晶,可得到CuCl2•2H2O晶体.
(2)在空气中直接加热CuCl2•2H2O晶体得不到纯的无水CuCl2,而是生成Cu(OH)Cl,写出相关的化学反应方程式:CuCl2•2H2O$\frac{\underline{\;\;△\;\;}}{\;}$Cu(OH)Cl+HCl↑+H2O.由CuCl2•2H2O晶体得到纯的无水CuCl2的合理方法是在干燥HCl气流中加热制得.
(3)某学习小组用“间接碘量法”测定含有CuCl2•2H2O晶体的试样(不含能与I-发生反应的氧化性杂质)的纯度,过程如下:取0.36g试样溶于水,加入过量KI固体,充分反应,生成白色CuI沉淀.过滤后,用0.100 0mol•L-1 Na2S2O3标准溶液滴定所得滤液,到达滴定终点时,消耗Na2S2O3标准溶液20.00mL.
①可选用淀粉作滴定指示剂,滴定终点的现象是蓝色变为无色,且在半分钟内无变化.
②CuCl2溶液与KI反应的离子方程式为2Cu2++4I-=2CuI↓+I2.
③该试样中CuCl2•2H2O的质量百分数为95.0%.
| 物质 | Cu(OH)2 | Fe(OH)3 | CuCl | CuI |
| Ksp | 2.2×10-20 | 2.6×10-39 | 1.7×10-7 | 1.3×10-12 |
(2)在空气中直接加热CuCl2•2H2O晶体得不到纯的无水CuCl2,而是生成Cu(OH)Cl,写出相关的化学反应方程式:CuCl2•2H2O$\frac{\underline{\;\;△\;\;}}{\;}$Cu(OH)Cl+HCl↑+H2O.由CuCl2•2H2O晶体得到纯的无水CuCl2的合理方法是在干燥HCl气流中加热制得.
(3)某学习小组用“间接碘量法”测定含有CuCl2•2H2O晶体的试样(不含能与I-发生反应的氧化性杂质)的纯度,过程如下:取0.36g试样溶于水,加入过量KI固体,充分反应,生成白色CuI沉淀.过滤后,用0.100 0mol•L-1 Na2S2O3标准溶液滴定所得滤液,到达滴定终点时,消耗Na2S2O3标准溶液20.00mL.
①可选用淀粉作滴定指示剂,滴定终点的现象是蓝色变为无色,且在半分钟内无变化.
②CuCl2溶液与KI反应的离子方程式为2Cu2++4I-=2CuI↓+I2.
③该试样中CuCl2•2H2O的质量百分数为95.0%.
9.外围电子构型为4d55s1的元素在周期表中的位置是( )
| A. | 第4周期第ⅠB族 | B. | 第5周期第ⅠB族 | C. | 第4周期第ⅥB族 | D. | 第5周期第ⅥB族 |
16.下列描述的过程中的能量变化与如图一致的是( )
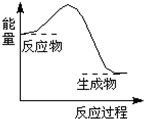

| A. | 反应物总键能比生成物总键能大 | B. | H-H键断裂 | ||
| C. | CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ | D. | 2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3 |
13.(1)如图1,在试管Ⅰ和Ⅱ中分别加入3mL稀盐酸(均足量),再将装有0.3g NaHCO3和0.3g Na2CO3粉末的小气球分别套在Ⅰ和Ⅱ的管口.将气球内的NaHCO3和Na2CO3同时倒入试管中,请回答下列问题:
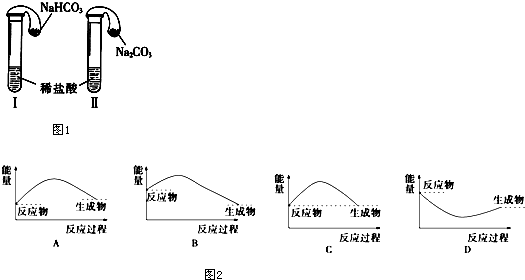
①试管Ⅰ和试管Ⅱ中发生反应的离子方程式分别为HCO3-+H+═CO2↑+H2O、CO32-+2H+═CO2↑+H2O.
②加入固体后,试管Ⅰ(填“Ⅰ”或“Ⅱ”)上的气球膨胀较快.
(2)为了研究Na2CO3、NaHCO3与盐酸的反应过程中的热效应,该同学继续进行了下列实验(每次实验各做3次平行实验,取平均值):
请你帮助填写相关内容:
①该研究报告的题目是碳酸钠、碳酸氢钠与盐酸反应过程中热效应的探究.
②通过上述实验可得出:
Na2CO3溶液和盐酸的反应是放热(填“吸热”或“放热”,下同)反应,对应的图象
为B(见图2)NaHCO3溶液和盐酸的反应是吸热反应,对应的图象为A.

①试管Ⅰ和试管Ⅱ中发生反应的离子方程式分别为HCO3-+H+═CO2↑+H2O、CO32-+2H+═CO2↑+H2O.
②加入固体后,试管Ⅰ(填“Ⅰ”或“Ⅱ”)上的气球膨胀较快.
(2)为了研究Na2CO3、NaHCO3与盐酸的反应过程中的热效应,该同学继续进行了下列实验(每次实验各做3次平行实验,取平均值):
| 序号 | 试剂1 | 试剂2 | 混合前温度 | 混合后的最高温度 |
| ① | 50mL水 | 2.5g NaHCO3固体 | 20℃ | 18.5℃ |
| ② | 50mL水 | 3.2g Na2CO3固体 | 20℃ | 24.3℃ |
| ③ | 50mL稀盐酸 | 2.5g NaHCO3固体 | 20℃ | 16.2℃ |
| ④ | 50mL稀盐酸 | 3.2g Na2CO3固体 | 20℃ | 25.1℃ |
①该研究报告的题目是碳酸钠、碳酸氢钠与盐酸反应过程中热效应的探究.
②通过上述实验可得出:
Na2CO3溶液和盐酸的反应是放热(填“吸热”或“放热”,下同)反应,对应的图象
为B(见图2)NaHCO3溶液和盐酸的反应是吸热反应,对应的图象为A.
14.下列有关叙述中不正确的是( )
| A. | 相同温度下,0.02 mol•L-1的醋酸溶液与0.01 mol•L-1的醋酸溶液中的c(H+)之比小于2:1 | |
| B. | 相同温度下,0.1 mol•L-1 (NH4)2SO4溶液与0.1 mol•L-1NH4NO3溶液中c(NH4+)之比大于2:1 | |
| C. | 在0.1 mol•L-1NaOH溶液中逐滴加入0.1 mol•L-1CH3COOH溶液,当溶液pH=7时,加入CH3COOH溶液的体积与NaOH溶液的体积比小于2:1 | |
| D. | 40℃时,pH=7的(NH4)2SO4与NH3•H2O的混合溶液中c(NH4+)与c(SO42-)之比小于2:1 |
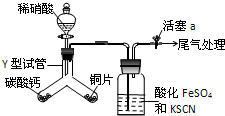 (1)为探究铜与稀硝酸反应的气态产物中是否含NO2,进行如下实验.
(1)为探究铜与稀硝酸反应的气态产物中是否含NO2,进行如下实验.