18.有一混合溶液中含有以下离子中的若干:K+、NH4+、Cl-、HCO3-、SO32-、SO42-、Ag+.现取等体积的两份溶液进行如下实验:
(1)第一份加入足量的NaOH溶液,无沉淀;加热,收集到标准状况下的气体336mL.
(2)第二份加入足量的用盐酸酸化的BaCl2溶液,产生2.33g白色沉淀,同时收集到标准状况下的气体336mL,该气体能使品红溶液褪色.
根据上述实验,下列推断正确的是( )
(1)第一份加入足量的NaOH溶液,无沉淀;加热,收集到标准状况下的气体336mL.
(2)第二份加入足量的用盐酸酸化的BaCl2溶液,产生2.33g白色沉淀,同时收集到标准状况下的气体336mL,该气体能使品红溶液褪色.
根据上述实验,下列推断正确的是( )
| A. | K+一定存在 | |
| B. | Ag+和Cl-一定不存在 | |
| C. | HCO3-一定不存在 | |
| D. | 混合溶液中一定有0.015 mol SO32- |
17.根据元素周期律,由列事实进行归纳推测,推测不合理的是事实( )
| 事实 | 推测 | |
| A | ${\;}_{12}^{\;}$Mg与水反应缓慢,${\;}_{20}^{\;}$Ca与水反应较快 | ${\;}_{56}^{\;}$Ba(DA族)与水反应会更快 |
| B | 是半导体材料,同族的Ge也是半导体材料 | Ⅳ族的元素都是半导体材料 |
| C | HCl在1500℃时分解,HI在230℃时分解 | HBr的分解温度介于二者之间 |
| D | Si与H2高温时反应,S与H2加热能反应 | P与H2在高温时能反应 |
| A. | A | B. | B | C. | C | D. | D |
16.下列离子方程式书写不正确的是( )
| A. | 单质铜与稀硝酸反应:Cu+2 H++2NO3-═Cu2++2 NO↑+H2O | |
| B. | NaOH溶液与足量的Ca(HCO3)2溶液反应:2HCO3-+2OH-+Ca2+═CaCO3↓+2H2O | |
| C. | 等物质的量的FeBr2和Cl2在溶液中的反应:2Fe2++2Br-+2Cl2═2Fe3++Br2+4Cl- | |
| D. | 氨水吸收少量的二氧化硫:2NH3•H2O+SO2═2NH4++SO32-+H2O |
15.下列物质中,含有非极性共价键的是( )
| A. | CaCl2 | B. | CO2 | C. | Na2O2 | D. | CH4 |
14.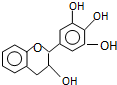 “茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂.其中没食子儿茶素(EGC)的结构如下图所示.关于EGC的下列叙述中正确的是( )
“茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂.其中没食子儿茶素(EGC)的结构如下图所示.关于EGC的下列叙述中正确的是( )
 “茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂.其中没食子儿茶素(EGC)的结构如下图所示.关于EGC的下列叙述中正确的是( )
“茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂.其中没食子儿茶素(EGC)的结构如下图所示.关于EGC的下列叙述中正确的是( )| A. | 分子中所有的原子共面 | |
| B. | 1molEGC与4molNaOH恰好完全反应 | |
| C. | 易发生氧化反应和取代反应,难发生加成反应 | |
| D. | 一定条件下的氧化产物能发生银镜反应 |
13.“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充电电池.如图为RFC工作原理示意图,有关说法正确的是( )


| A. | 转移0.1mol电子时,a电极产生1.12LH2 | |
| B. | b电极上发生的电极反应是:2H2O+2e-=H2↑+2OH- | |
| C. | c电极上进行还原反应,B电池中的H+可以通过隔膜进入A池 | |
| D. | d电极上发生的电极反应是:O2+4H++4e-=2H2O |
12.草酸是二元中强酸,草酸氢钠溶液显酸性.常温下,向10mL 0.01mol/L NaHC2O4溶液中滴加0.01mol/L NaOH溶液,随着NaOH溶液体积的增加,溶液中离子浓度关系正确的是( )
| A. | V(NaOH)=0时,c(H+)=1×10-2 mol/L | |
| B. | V(NaOH)<10 mL时,可能存在c(Na+)=2c(C2O42-)+c(HC2O4-) | |
| C. | V(NaOH)=10mL时,c(H+)=1×10-7 mol/L | |
| D. | V(NaOH)>10 mL时,c(Na+)>c(HC2O4-)>c(C2O42-) |
11.如图所示,△H1=-393.5kJ•mol-1,△H2=-395.4kJ•mol-1,下列说法或表示式正确的是( )
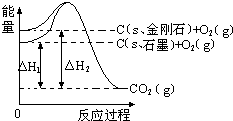

| A. | 石墨和金刚石的转化是物理变化 | |
| B. | C(s、石墨)═C(s、金刚石)△H=+1.9 kJ•mol-1 | |
| C. | 金刚石的稳定性强于石墨 | |
| D. | 1 mol石墨的总键能比1 mol金刚石的总键能小1.9 kJ |
9.现有部分短周期元素的性质或原子结构如下表:
(1)A的气态氢化物的化学式是H2S,元素B(含8个中子)的一种同位素可测定文物年代,这种同位素的符号是146C.
(2)写出元素F的离子结构示意图 .
.
(3)写出G元素最高价氧化物对应的水化物的化学式是Al(OH)3.
(4)元素D与元素A相比,非金属性较强的是Cl(用元素符号表示),下列表述中能证明这一事实的是b.
a.常温下D的单质和A的单质状态不同
b.D的氢化物比A的氢化物稳定
c.一定条件下D和A的单质都能与氢氧化钠溶液反应
(5)A、B、C、D四种元素的最高价氧化物对应的水化物中化学性质明显不同于其他三种酸的是H2CO3,理由是碳酸属于弱酸,其它三种酸均为强酸.
(6)C、E、F、G四种元素的单质中化学性质明显不同于其他三种单质的是Al,理由Al具有金属性或是金属.
(7)F的阴离子和G的阳离子的半径大小比较:F->Al3+(用离子符号表示)
(8)A、D的简单离子的还原性强弱:S2->Cl-(用离子符号表示)
0 167726 167734 167740 167744 167750 167752 167756 167762 167764 167770 167776 167780 167782 167786 167792 167794 167800 167804 167806 167810 167812 167816 167818 167820 167821 167822 167824 167825 167826 167828 167830 167834 167836 167840 167842 167846 167852 167854 167860 167864 167866 167870 167876 167882 167884 167890 167894 167896 167902 167906 167912 167920 203614
| 元素编号 | 元素性质或原子结构 |
| A | 室温下其单质呈粉末状黄色固体,加热易熔化.该单质在氧气中燃烧,发出明亮的蓝紫色火焰 |
| B | 最外层电子数是次外层电子数的2倍 |
| C | 最外层电子数比次外层电子数多3个 |
| D | 元素最高正价是+7价 |
| E | 主族元素中得电子能力最强 |
| F | 空气的主要成分之一,其某种同素异形体是保护地球地表环境的重要屏障 |
| G | 第3周期元素的简单离子中半径最小 |
(2)写出元素F的离子结构示意图
 .
.(3)写出G元素最高价氧化物对应的水化物的化学式是Al(OH)3.
(4)元素D与元素A相比,非金属性较强的是Cl(用元素符号表示),下列表述中能证明这一事实的是b.
a.常温下D的单质和A的单质状态不同
b.D的氢化物比A的氢化物稳定
c.一定条件下D和A的单质都能与氢氧化钠溶液反应
(5)A、B、C、D四种元素的最高价氧化物对应的水化物中化学性质明显不同于其他三种酸的是H2CO3,理由是碳酸属于弱酸,其它三种酸均为强酸.
(6)C、E、F、G四种元素的单质中化学性质明显不同于其他三种单质的是Al,理由Al具有金属性或是金属.
(7)F的阴离子和G的阳离子的半径大小比较:F->Al3+(用离子符号表示)
(8)A、D的简单离子的还原性强弱:S2->Cl-(用离子符号表示)
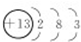 .
.