题目内容
16.下列离子方程式书写不正确的是( )| A. | 单质铜与稀硝酸反应:Cu+2 H++2NO3-═Cu2++2 NO↑+H2O | |
| B. | NaOH溶液与足量的Ca(HCO3)2溶液反应:2HCO3-+2OH-+Ca2+═CaCO3↓+2H2O | |
| C. | 等物质的量的FeBr2和Cl2在溶液中的反应:2Fe2++2Br-+2Cl2═2Fe3++Br2+4Cl- | |
| D. | 氨水吸收少量的二氧化硫:2NH3•H2O+SO2═2NH4++SO32-+H2O |
分析 A.发生氧化还原反应,生成硝酸铜、NO和水,电子、电荷不守恒;
B.NaOH完全反应,生成碳酸钙、碳酸氢钠、水;
C.等物质的量反应,亚铁离子全部被氧化,溴离子一半被氧化;
D.反应生成亚硫酸铵和水.
解答 解:A.单质铜与稀硝酸反应的离子反应为3Cu+8H++2NO3-═3Cu2++2 NO↑+4H2O,故A错误;
B.NaOH溶液与足量的Ca(HCO3)2溶液反应的离子反应为HCO3-+OH-+Ca2+═CaCO3↓+H2O,故B错误;
C.等物质的量的FeBr2和Cl2在溶液中的反应的离子反应为2Fe2++2Br-+2Cl2═2Fe3++Br2+4Cl-,遵循电子守恒,故C正确;
D.氨水吸收少量的二氧化硫的离子反应为2NH3•H2O+SO2═2NH4++SO32-+H2O,故D正确;
故选AB.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重与量有关的离子反应、氧化还原反应的离子反应考查,注意离子反应中保留化学式的物质,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
5.锌电池有望代替铅蓄电池,它的构成材料是锌、空气、某种电解质溶液,发生的总反应式是2Zn+O2=2ZnO.下列有关它的说法正确的是( )
| A. | 锌为电池负极,发生氧化反应 | |
| B. | 电解质溶液是酸性溶液 | |
| C. | 电池工作时,氧气与锌直接化合,生成氧化锌 | |
| D. | 负极发生的反应是:Zn-2e-+H2O=ZnO+2H+ |
7.下列各选项能说明分子式为C4H6的某烃是 ,而不是
,而不是 的事实是( )
的事实是( )
 ,而不是
,而不是 的事实是( )
的事实是( )| A. | 燃烧有浓烟 | |
| B. | 能使酸性高锰酸钾溶液褪色 | |
| C. | 所在原子不在同一平面上 | |
| D. | 与足量溴水反应,生成物中只有2个碳原子上有溴原子 |
4.根据化学反应的实质是旧键断裂新键形成这一事实,下列变化不属于化学反应的是( )
| A. | 白磷在260℃时转化为红磷 | B. | 石墨在高温下转化为金刚石 | ||
| C. | NaCl熔化 | D. | 氧化钙吸水 |
11.如图所示,△H1=-393.5kJ•mol-1,△H2=-395.4kJ•mol-1,下列说法或表示式正确的是( )
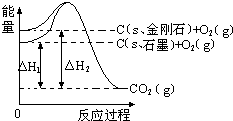

| A. | 石墨和金刚石的转化是物理变化 | |
| B. | C(s、石墨)═C(s、金刚石)△H=+1.9 kJ•mol-1 | |
| C. | 金刚石的稳定性强于石墨 | |
| D. | 1 mol石墨的总键能比1 mol金刚石的总键能小1.9 kJ |
1.已知单质A能从溶液中置换出单质B.下列分析不正确的是( )
| A. | 当A、B都是金属,A的还原性一定比B强 | |
| B. | 当A、B都是非金属时,A的非金属性一定比B强 | |
| C. | 当A是金属时,B可能是金属,也可能是非金属 | |
| D. | 当A是非金属时,B可能是非金属,也可能是金属 |
8.描述CH3-CH=CH-C≡C-CF3分子结构的下列叙述中,正确的是( )
| A. | 6个碳原子有可能都在同一直线上 | |
| B. | 在同一直线上的碳原子可能为4个 | |
| C. | 分子中所有原子有可能都在同一平面上 | |
| D. | 6个碳原子不可能都在同一平面上 |
5.关于10mL 0.1mol•L-1的NH3•H2O溶液,下列说法正确的是( )
| A. | 25℃时,若溶液的pH=11,则Kb(NH3•H2O)=1×10-6 | |
| B. | 向溶液中加入少量CH3COONa固体,溶液中$\frac{c(N{H}_{3}.{H}_{2}O)}{c(N{H}_{4}^{+})}$的值变小 | |
| C. | 向溶液中加入10 mL 0.1 mol•L-1盐酸,所得溶液中离子浓度大小顺序为:c(NH4+)>(Cl-)>c(H+)>c(OH-) | |
| D. | 向溶液中加入5 mL 0.1 mol•L-1盐酸,所得溶液中离子的浓度一定符合:c(NH4+)+c(H+)=c(Cl-)+c(OH-) |
6.下列叙述不正确的是( )
| A. | 根据一次能源与二次能源的划分,氢气为二次能源 | |
| B. | 空气、水、煤、天然气均为可再生资源 | |
| C. | 镁条燃烧时将部分化学能转化为光能 | |
| D. | 在火力发电时,化学能转化为热能的过程实际上是氧化还原反应发生的过程,伴随着能量的变化 |