17.按电子排布,可把周期表里的元素划分成5个区,以下元素属于P区的是( )
| A. | Fe | B. | Mg | C. | P | D. | Na |
16.下列溶液中的离子反应表达正确的是( )
| A. | 将金属钠投入水中:Na+2H2O═Na++2OH-+H2↑ | |
| B. | 大理石与醋酸的反应:CaCO3+2H+═Ca2++CO2↑+H2O | |
| C. | 三氯化铁溶液中加入铜粉:Cu+Fe3+═Cu2++Fe2+ | |
| D. | 氯化铝溶液中加入过量的氨水:Al3++3NH3•H2O═Al(OH)3↓+3NH${\;}_{4}^{+}$ |
14.下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:
(1)⑦是什么元素Al(用元素符号表示).
(2)请写出⑨的原子结构示意图 .
.
(3)②、③、④、⑤的半径从大到小的顺序是C>N>O>F(用元素符号表示).
(4)⑥与⑦两种元素金属性强弱顺序为:⑥>⑦(填“>”或“<”或“=”)
(5)①与③形成的最简单化合物的电子式: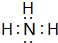
(6)请写出⑧元素最高价氧化物的化学式:SO3.⑥的最高价氧化物对应的水化物与⑦的最高价氧化物对应的水化物相互反应的化学方程式:Al(OH)3+NaOH=NaAlO2+2H2O.
| 族 周期 | IA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ | ||||
(2)请写出⑨的原子结构示意图
 .
.(3)②、③、④、⑤的半径从大到小的顺序是C>N>O>F(用元素符号表示).
(4)⑥与⑦两种元素金属性强弱顺序为:⑥>⑦(填“>”或“<”或“=”)
(5)①与③形成的最简单化合物的电子式:
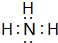
(6)请写出⑧元素最高价氧化物的化学式:SO3.⑥的最高价氧化物对应的水化物与⑦的最高价氧化物对应的水化物相互反应的化学方程式:Al(OH)3+NaOH=NaAlO2+2H2O.
13.化学反应A(g)+3B(g)=2C(g)+2D(g),下列四个选项是不同的情况下测得的不同物质的反应速率,其中表示该化学反应的反应速率最快的是( )
| A. | υ(A)=0.20mol/(L•min) | B. | υ(B)=0.45 mol/(L•min) | ||
| C. | υ(C)=0.30 mol/(L•min) | D. | υ(D)=0.35 mol/(L•min) |
12.下列反应的离子方程式正确的是( )
| A. | NaHCO3溶液与盐酸:CO32-+2 H+=H2O+CO2↑ | |
| B. | 硝酸银溶液与铜:Cu+Ag+=Cu2++Ag | |
| C. | 金属钾与水反应:K+H2O═K++OH-+H2↑ | |
| D. | 用醋酸除水垢:2CH3COOH+CaCO3=Ca2++2CH3COO-+H2O+CO2↑ |
11.下列说法正确的是( )
| A. | 含有共价键的化合物一定是共价化合物 | |
| B. | 分子中只有共价键的化合物一定是共价化合物 | |
| C. | 由共价键形成的一定是共价化合物分子 | |
| D. | 只有非金属原子间才能形成共价键 |
9.下列不属于影响离子晶体结构的因素是 ( )
| A. | 晶体中阴、阳离子的半径比 | B. | 离子晶体的晶格能 | ||
| C. | 晶体中阴、阳离子的电荷比 | D. | 离子键的纯粹程度 |
8.下列有关实验的叙述不正确的是( )
0 167664 167672 167678 167682 167688 167690 167694 167700 167702 167708 167714 167718 167720 167724 167730 167732 167738 167742 167744 167748 167750 167754 167756 167758 167759 167760 167762 167763 167764 167766 167768 167772 167774 167778 167780 167784 167790 167792 167798 167802 167804 167808 167814 167820 167822 167828 167832 167834 167840 167844 167850 167858 203614
| A. | 某气体能使湿润的红色石蕊试纸变蓝,该气体水溶液一定显碱性 | |
| B. | 碘水与碘化钾淀粉试纸作用出现蓝色,说明碘具有氧化性 | |
| C. | 往饱和Na2CO3溶液中通入CO2有固体析出,说明NaHCO3溶解度小于Na2CO3 | |
| D. | 同温下,等物质的量浓度的Al2(SO4)3比MgSO4溶液的pH小,说明镁比铝的金属性强 |
