题目内容
16.下列溶液中的离子反应表达正确的是( )| A. | 将金属钠投入水中:Na+2H2O═Na++2OH-+H2↑ | |
| B. | 大理石与醋酸的反应:CaCO3+2H+═Ca2++CO2↑+H2O | |
| C. | 三氯化铁溶液中加入铜粉:Cu+Fe3+═Cu2++Fe2+ | |
| D. | 氯化铝溶液中加入过量的氨水:Al3++3NH3•H2O═Al(OH)3↓+3NH${\;}_{4}^{+}$ |
分析 A.电荷不守恒;
B.醋酸为弱电解质,应保留化学式;
C.电荷不守恒;
D.氯化铝溶液中加入过量的氨水反应生成氢氧化铝和氯化铵.
解答 解:A.金属钠投入水中反应的离子方程式:2Na+2H2O═2Na++2OH-+H2↑,故A错误;
B.大理石与醋酸的反应,离子方程式:CaCO3+2CH3COOH═Ca2++CO2↑+H2O+2CH3COO-,故B错误;
C.三氯化铁溶液中加入铜粉,离子方程式:Cu+2Fe3+═Cu2++2Fe2+,故C错误;
D.氯化铝溶液中加入过量的氨水,离子方程式:Al3++3NH3•H2O═Al(OH)3↓+3NH${\;}_{4}^{+}$,故D正确;
故选:D.
点评 本题考查了离子方程式的正误判断,书写离子方程式应注意遵循客观事实、遵循原子个数、电荷数守恒规律,题目难度不大.

练习册系列答案
相关题目
6.在周期表主族元素中,X元素位于第二周期,且分别与Y、Z、W三元素相邻,X、Y的原子序数之和等于Z的原子序数;这四种元素原子的最外层电子数之和为20.下列判断正确的是( )
| A. | 原子序数:Z>Y>X>W | |
| B. | X、Y、Z、W形成的单质最多有6种 | |
| C. | X元素最高价氧化物对应水化物的化学式为:H2XO3 | |
| D. | 四种元素的气态氢化物中,W的气态氢化物最稳定 |
7.下列叙述错误的是( )
| A. | 活性炭、SO2、Na2O2都能使品红溶液褪色,但原理不同 | |
| B. | FeO在空气中受热会迅速转变为Fe2O3 | |
| C. | Na2SiO3溶液俗称水玻璃,可用于制备硅胶和木材防火剂 | |
| D. | 制作“毒豆芽”所用的亚硝酸钠、“小苏打水”中的碳酸氢钠都属于钠盐 |
4.下列物质属于纯净物的是( )
| A. | 乙烷 | B. | 聚乙烯 | C. | 汽油 | D. | 天然气 |
11.下列说法正确的是( )
| A. | 含有共价键的化合物一定是共价化合物 | |
| B. | 分子中只有共价键的化合物一定是共价化合物 | |
| C. | 由共价键形成的一定是共价化合物分子 | |
| D. | 只有非金属原子间才能形成共价键 |
1.液化石油气是石油化工生产过程中的一种副产品,也是常用的家用燃料,它的主要成分是丙烷、丁烷、丙烯、丁烯.下列说法中不正确的是( )
| A. | 丙烷和丁烷互为同系物 | |
| B. | 丙烯和丁烯互为同系物 | |
| C. | 丙烷和丁烷中碳元素的质量分数相同 | |
| D. | 丙烯和丁烯中碳元素的质量分数相同 |
5.过量的下列溶液与水杨酸( )反应能得到化学式为C7H5O3Na的是( )
)反应能得到化学式为C7H5O3Na的是( )
 )反应能得到化学式为C7H5O3Na的是( )
)反应能得到化学式为C7H5O3Na的是( )| A. | NaHCO3溶液 | B. | Na2CO3溶液 | C. | NaOH溶液 | D. | NaCl溶液 |
19.下列关于电解质溶液的叙述正确的是( )
| A. | pH均为4的H2SO4、NH4Cl溶液中,水的电离程度相同 | |
| B. | 等pH的NaOH溶液与NH3•H2O 稀释后pH的变化如右图所示,则曲线I表示的是NaOH溶液的稀释 | |
| C. | 1mol/LNa2CO3溶液中存在:c(Na+)=2c(CO32- )+2c(HCO3-) | |
| D. | 向某温度的氨水中通入盐酸,则氨水的电离常数增大 |
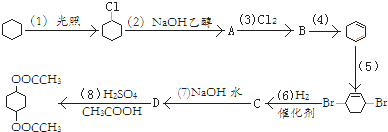
 ,取代反应
,取代反应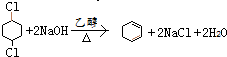 ,消去反应
,消去反应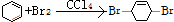 ,加成反应
,加成反应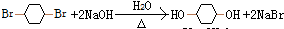 ,取代反应(水解反应)
,取代反应(水解反应)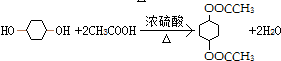 ,取代反应(酯化反应).
,取代反应(酯化反应).