题目内容
9.下列不属于影响离子晶体结构的因素是 ( )| A. | 晶体中阴、阳离子的半径比 | B. | 离子晶体的晶格能 | ||
| C. | 晶体中阴、阳离子的电荷比 | D. | 离子键的纯粹程度 |
分析 离子晶体的结构类型取决于晶体中阴阳离子的半径比、阴阳离子的电荷比和离子键的纯粹程度,据此分析.
解答 解:影响离子晶体结构的因素是几何因素(即晶体中正负离子的半径比)、电荷因素(阴阳离子的电荷比)、键性因素(即离子键的纯粹程度),晶格能是最能反映离子晶体稳定性的数据,而不是影响离子晶体结构的因素.
故选B.
点评 本题考查了影响离子晶体结构的因素,题目难度不大,注意对基础知识的记忆和掌握.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案
相关题目
20.某饱和一元酸跟足量金属钠反应生成0.5gH2.等量的该醇经充分燃烧后生成H2O36g.则该醇应是( )
| A. | 甲醇 | B. | 乙醇 | C. | 丙醇 | D. | 丁醇 |
17.几种短周期元素的原子半径及主要化合价见表:根据表中信息,判断以下说法正确的是( )
| 元素符号 | X | Y | Z | R | T |
| 原子半径(nm) | 0.160 | 0.111 | 0.104 | 0.143 | 0.066 |
| 主要化合价 | +2 | +2 | -2,+4,+6 | +3 | -2 |
| A. | 离子的还原性:T2->Z2- | |
| B. | 离子半径:Z2->X2+ | |
| C. | Y的原子序数大于X | |
| D. | X和Y的最高价氧化物的水化物的碱性:Y>X |
4.下列物质属于纯净物的是( )
| A. | 乙烷 | B. | 聚乙烯 | C. | 汽油 | D. | 天然气 |
14.下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:
(1)⑦是什么元素Al(用元素符号表示).
(2)请写出⑨的原子结构示意图 .
.
(3)②、③、④、⑤的半径从大到小的顺序是C>N>O>F(用元素符号表示).
(4)⑥与⑦两种元素金属性强弱顺序为:⑥>⑦(填“>”或“<”或“=”)
(5)①与③形成的最简单化合物的电子式: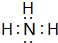
(6)请写出⑧元素最高价氧化物的化学式:SO3.⑥的最高价氧化物对应的水化物与⑦的最高价氧化物对应的水化物相互反应的化学方程式:Al(OH)3+NaOH=NaAlO2+2H2O.
| 族 周期 | IA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ | ||||
(2)请写出⑨的原子结构示意图
 .
.(3)②、③、④、⑤的半径从大到小的顺序是C>N>O>F(用元素符号表示).
(4)⑥与⑦两种元素金属性强弱顺序为:⑥>⑦(填“>”或“<”或“=”)
(5)①与③形成的最简单化合物的电子式:
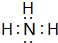
(6)请写出⑧元素最高价氧化物的化学式:SO3.⑥的最高价氧化物对应的水化物与⑦的最高价氧化物对应的水化物相互反应的化学方程式:Al(OH)3+NaOH=NaAlO2+2H2O.
1.液化石油气是石油化工生产过程中的一种副产品,也是常用的家用燃料,它的主要成分是丙烷、丁烷、丙烯、丁烯.下列说法中不正确的是( )
| A. | 丙烷和丁烷互为同系物 | |
| B. | 丙烯和丁烯互为同系物 | |
| C. | 丙烷和丁烷中碳元素的质量分数相同 | |
| D. | 丙烯和丁烯中碳元素的质量分数相同 |
18.下列过程中化学键没有被破坏的是( )
| A. | 二氧化碳溶于水 | |
| B. | 氯化钠溶于水 | |
| C. | 水沸腾汽化 | |
| D. | 煤矿中瓦斯(主要成分是甲烷)遇火爆炸 |
 .
.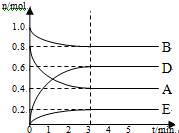 某温度T℃下,在某个固定容积为2.0L的密闭容器内,在时按右图所示发生反应:其中A、B、D为气体,E为固体.
某温度T℃下,在某个固定容积为2.0L的密闭容器内,在时按右图所示发生反应:其中A、B、D为气体,E为固体.