题目内容
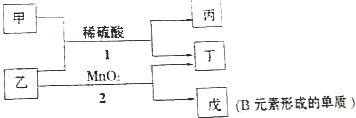
10.硫酸亚铁铵在500℃时隔绝空气加热能完全分解.回答下列问题:(1)硫酸亚铁铵隔绝空气加热能完全分解,发生了氧化还原反应,固体产物可能有FeO和Fe2O3,气体产物可能有NH3、SO3、H2O、N2和SO2.
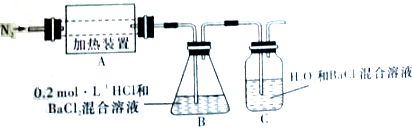
(2)为检验加热分解后产物的成分并测定部分气体产物的量,设计如下实验装置进行实验,加热A中的硫酸亚铁铵至分解完全.A中的固体充分加热较长时间后,通入氮气,目的是使分解产生的气体在B、C中被吸收充分.
分析 (1)氮元素和铁元素化合价升高,根据在氧化还原反应中化合价有升必有降;
(2)A中固体充分加热较长时间后,通入氮气目的是使分解生成的气体在BC装置中完全吸收.
解答 解:(1)氮元素和铁元素化合价升高,根据在氧化还原反应中化合价有升必有降,化合价降低的应该是硫,所以气体产物中还可能有SO2;
故答案为:SO2;
(2)为检验加热分解后产物的成分并测定部分气体产物的量,A中固体充分加热较长时间后生成气体,若要测定生成的气体,需要把气体全部赶入B、C中,所以通入氮气目的是使分解生成的气体在BC装置中完全吸收;
故答案为:使分解产生的气体在B、C中被吸收充分.
点评 本题考查性质实验方案设计,明确物质的性质、实验原理是解本题关键,侧重考查学生分析问题、解答问题能力,熟练掌握元素化合物知识,题目难度不大.

练习册系列答案
 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案
相关题目
18.下列各物质中所有原子都满足最外层8电子结构的是①N2 ②Cl2 ③CO2 ④PCl5⑤H2O( )
| A. | 全部 | B. | ①②③⑤ | C. | ①②③ | D. | ①②③④ |
5.分别燃烧等物质的量的下列各组物质,其中消耗氧气量相等的是( )
①C2H2 与CH3CHO ②C7H8与C6H12 ③C2H2与C6H6④HCOOCH3与CH3COOH.
①C2H2 与CH3CHO ②C7H8与C6H12 ③C2H2与C6H6④HCOOCH3与CH3COOH.
| A. | ①②③④ | B. | ①②④ | C. | ①④ | D. | ②④ |
2.胡椒酚(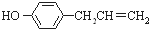 )是植物挥发油中的一种成分,1mol胡椒酚最多可与a mol H2发生反应、最多可与b mol Br2在水溶液中发生反应,则a、b分别是( )
)是植物挥发油中的一种成分,1mol胡椒酚最多可与a mol H2发生反应、最多可与b mol Br2在水溶液中发生反应,则a、b分别是( )
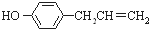 )是植物挥发油中的一种成分,1mol胡椒酚最多可与a mol H2发生反应、最多可与b mol Br2在水溶液中发生反应,则a、b分别是( )
)是植物挥发油中的一种成分,1mol胡椒酚最多可与a mol H2发生反应、最多可与b mol Br2在水溶液中发生反应,则a、b分别是( )| A. | 4 3 | B. | 4 2 | C. | 3 3 | D. | 3 2 |
13.某化学小组为了研究外界条件对化学反应速率的影响,进行了如下实验:
【实验原理】2KMnO4+5H2C2O4+3H2SO4═K2SO4+2MnSO4+10CO2↑+8H2O
【实验内容及记录】
实验1、2、3、4按下列表格药品用量实验,并都加水稀释至10mL,假设加水后两者开始反应(下面实验同),均在室温下观察溶液颜色褪去时间,并记录如下:
请回答:
(1)根据上表中的实验数据,可以得到的结论是其他条件相同时,增大KMnO4浓度反应速率增大.
(2)利用实验1中数据计算,用KMnO4的浓度变化表示从反应开始至颜色褪色这段时间该反应的反应速率为:
υ(KMnO4)=1.5×10-2mol/(L•min).
(3)该小组同学根据经验绘制了n(Mn2+) 随时间变化趋势的示意图,如图1所示.但有同学查阅已有的实验资料发现,该实验过程中n(Mn2+) 随时间变化的趋势应如图2所示.该小组同学根据图2所示信息提出了新的假设,并继续进行实验探究.

①该小组同学提出的假设是生成物中的MnSO4为该反应的催化剂(或Mn2+对该反应有催化作用).
②请你帮助该小组同学完成实验方案,并填写表中空白.
③若该小组同学提出的假设成立,应观察到的现象是与实验1比较,溶液褪色所需时间短(或所用时间(t)小于4min).
【实验原理】2KMnO4+5H2C2O4+3H2SO4═K2SO4+2MnSO4+10CO2↑+8H2O
【实验内容及记录】
实验1、2、3、4按下列表格药品用量实验,并都加水稀释至10mL,假设加水后两者开始反应(下面实验同),均在室温下观察溶液颜色褪去时间,并记录如下:
| 实验编号 | 室温下,试管中所加试剂及其用量/mL | 室温下溶液颜色褪至无色所需时间/min | ||
| 0.6 mol/L H2C2O4溶液 | 0.2 mol/L KMnO4溶液 | 3 mol/L 稀硫酸 | ||
| 1 | 3.0 | 3.0 | 2.0 | 4.0 |
| 2 | 3.0 | 2.0 | 2.0 | 5.2 |
| 3 | 3.0 | 1.0 | 2.0 | 6.4 |
(1)根据上表中的实验数据,可以得到的结论是其他条件相同时,增大KMnO4浓度反应速率增大.
(2)利用实验1中数据计算,用KMnO4的浓度变化表示从反应开始至颜色褪色这段时间该反应的反应速率为:
υ(KMnO4)=1.5×10-2mol/(L•min).
(3)该小组同学根据经验绘制了n(Mn2+) 随时间变化趋势的示意图,如图1所示.但有同学查阅已有的实验资料发现,该实验过程中n(Mn2+) 随时间变化的趋势应如图2所示.该小组同学根据图2所示信息提出了新的假设,并继续进行实验探究.

①该小组同学提出的假设是生成物中的MnSO4为该反应的催化剂(或Mn2+对该反应有催化作用).
②请你帮助该小组同学完成实验方案,并填写表中空白.
| 实验编号 | 室温下,试管中所加试剂及其用量/mL | 再向试管中加入少量固体 | 室温下溶液颜色褪至无色所需时间/min | ||
| 0.6 mol/L H2C2O4溶液 | 0.2 mol/L KMnO4溶液 | 3 mol/L 稀硫酸 | |||
| 4 | 3.0 | 3.0 | 2.0 | t | |
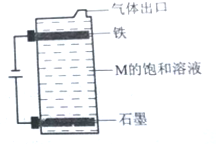 A、B、C、D、E为原子序数依次增大的短周期元素.A、C处于同一主族,C、D、E处于同一周期;A、B组成的气体X能使湿润的红色石蕊试纸变蓝.C在短周期元素中金属性最强,E原子的最外层电子数是A、B、C原子最外层电子数之和,E的单质与x反应能生成溶于水呈强酸性的化合物Z,同时生成B的单质,D的单质既能与C的最高价氧化物的水溶液反应,也能与Z的水溶液反应;C、E可组成化合物M.
A、B、C、D、E为原子序数依次增大的短周期元素.A、C处于同一主族,C、D、E处于同一周期;A、B组成的气体X能使湿润的红色石蕊试纸变蓝.C在短周期元素中金属性最强,E原子的最外层电子数是A、B、C原子最外层电子数之和,E的单质与x反应能生成溶于水呈强酸性的化合物Z,同时生成B的单质,D的单质既能与C的最高价氧化物的水溶液反应,也能与Z的水溶液反应;C、E可组成化合物M.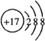 .
.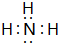 ;
;