10. CO的应用和治理是当今社会的热点问题.
CO的应用和治理是当今社会的热点问题.
(1)CO能导致镍系催化剂中毒,工业上常用SO2除去原料气中少量CO,生成物为固体S和CO2.写出该反应的化学方程式为2CO+SO2=2CO2+S.
(2)上述反应中,每减少2.24L气体(标准状况下),转移电子数为0.4NA.
CO工业上可用于高炉炼铁,发生如下反应:$\frac{1}{3}$Fe2O3(s)+CO(g)?$\frac{2}{3}$Fe(s)+CO2(g),
已知该反应在不同温度下的平衡常数如表:
(3)下列说法不正确的是cd(选填序号)
a.该反应是一个放热反应
b.该反应的平衡常数表达式是K=$\frac{c(C{O}_{2})}{c(CO)}$
c.其他条件不变,向平衡体系充入CO2气体,K值减小
d.当K值等于1时,反应达到平衡
(4)欲提高CO的平衡转化率,促进Fe2O3的转化,可采取的措施是a(选填序号)
a.及时吸收或移出CO2
b.增大反应体系的压强
c.用更高效的催化剂
d.粉碎矿石,增大接触面积
高炉炼铁产生的废气中的CO可进行回收,使其在一定条件下和H2反应制备甲醇:CO(g)+2H2(g)?CH3OH(g)+Q
(5)从上图可以看出,反应开始到平衡,反应速率v(H2)=0.15mol/(L•min).
(6)甲醇氧化可生成甲酸,能使0.1mol/L的甲酸溶液的电离度与pH值都增大的是ad(选填序号)
a.加水稀释 b.加入少量甲酸钠固体 c.通氯化氢 d.加入少量苛性钠固体.
 CO的应用和治理是当今社会的热点问题.
CO的应用和治理是当今社会的热点问题.(1)CO能导致镍系催化剂中毒,工业上常用SO2除去原料气中少量CO,生成物为固体S和CO2.写出该反应的化学方程式为2CO+SO2=2CO2+S.
(2)上述反应中,每减少2.24L气体(标准状况下),转移电子数为0.4NA.
CO工业上可用于高炉炼铁,发生如下反应:$\frac{1}{3}$Fe2O3(s)+CO(g)?$\frac{2}{3}$Fe(s)+CO2(g),
已知该反应在不同温度下的平衡常数如表:
| 温度/℃ | 1000 | 1150 | 1300 |
| 平衡常数 | 4.0 | 3.7 | 3.5 |
a.该反应是一个放热反应
b.该反应的平衡常数表达式是K=$\frac{c(C{O}_{2})}{c(CO)}$
c.其他条件不变,向平衡体系充入CO2气体,K值减小
d.当K值等于1时,反应达到平衡
(4)欲提高CO的平衡转化率,促进Fe2O3的转化,可采取的措施是a(选填序号)
a.及时吸收或移出CO2
b.增大反应体系的压强
c.用更高效的催化剂
d.粉碎矿石,增大接触面积
高炉炼铁产生的废气中的CO可进行回收,使其在一定条件下和H2反应制备甲醇:CO(g)+2H2(g)?CH3OH(g)+Q
(5)从上图可以看出,反应开始到平衡,反应速率v(H2)=0.15mol/(L•min).
(6)甲醇氧化可生成甲酸,能使0.1mol/L的甲酸溶液的电离度与pH值都增大的是ad(选填序号)
a.加水稀释 b.加入少量甲酸钠固体 c.通氯化氢 d.加入少量苛性钠固体.
9. 如图所示甲、乙两个装置,所盛溶液体积和浓度均相同且足量,电极铝和镁都已除去表面氧化膜.当两装置电路中通过的电子都是1mol时,下列说法不正确的是( )
如图所示甲、乙两个装置,所盛溶液体积和浓度均相同且足量,电极铝和镁都已除去表面氧化膜.当两装置电路中通过的电子都是1mol时,下列说法不正确的是( )
 如图所示甲、乙两个装置,所盛溶液体积和浓度均相同且足量,电极铝和镁都已除去表面氧化膜.当两装置电路中通过的电子都是1mol时,下列说法不正确的是( )
如图所示甲、乙两个装置,所盛溶液体积和浓度均相同且足量,电极铝和镁都已除去表面氧化膜.当两装置电路中通过的电子都是1mol时,下列说法不正确的是( )| A. | 溶液的质量减小程度:乙<甲 | |
| B. | 溶液的导电能力变化:甲>乙 | |
| C. | 甲中阴极和乙中镁电极上析出物质质量:甲=乙 | |
| D. | 电极反应式:甲中阳极:2Cl--2e→Cl2↑,乙中正极:Cu2++2e→Cu |
8.下列有关侯氏制碱法的描述正确的是( )
0 167571 167579 167585 167589 167595 167597 167601 167607 167609 167615 167621 167625 167627 167631 167637 167639 167645 167649 167651 167655 167657 167661 167663 167665 167666 167667 167669 167670 167671 167673 167675 167679 167681 167685 167687 167691 167697 167699 167705 167709 167711 167715 167721 167727 167729 167735 167739 167741 167747 167751 167757 167765 203614
| A. | 该反应条件下,碳酸氢钠难溶于水 | B. | 氨气和二氧化碳均来自合成氨工厂 | ||
| C. | 侯氏制碱法实现了对氨气循环利用 | D. | 生产时,应先通二氧化碳再通氨气 |
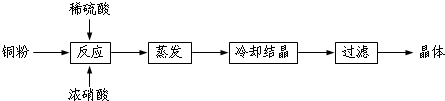
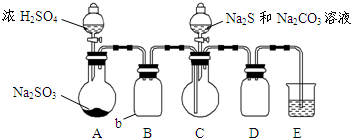 硫代硫酸钠是一种重要的化工产品.某兴趣小组拟制备硫代硫酸钠晶体(Na2S2O3•5H2O).
硫代硫酸钠是一种重要的化工产品.某兴趣小组拟制备硫代硫酸钠晶体(Na2S2O3•5H2O).
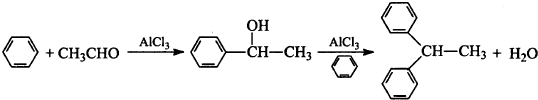
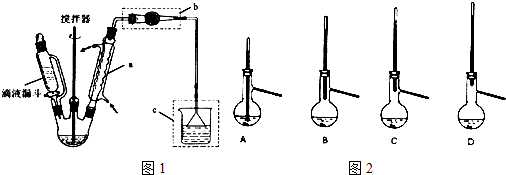
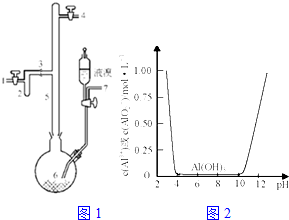 利用废铝箔(主要成分为Al、少量的Fe、Si等)既可制取有机合成催化剂AlBr3又可制取净水剂硫酸铝晶体.
利用废铝箔(主要成分为Al、少量的Fe、Si等)既可制取有机合成催化剂AlBr3又可制取净水剂硫酸铝晶体.


 )发生缩聚反应产物的结构简式为
)发生缩聚反应产物的结构简式为 ;P物质的钠盐在适当条件下氧化为芳香醛Q,则Q与银氨溶液发生反应的化学方程式为
;P物质的钠盐在适当条件下氧化为芳香醛Q,则Q与银氨溶液发生反应的化学方程式为 .
.
 ;A、B可以发生类似①的反应生成有机物Ⅰ,则该反应的化学方程式为
;A、B可以发生类似①的反应生成有机物Ⅰ,则该反应的化学方程式为 .
.