4.对于工业合成氨反应:N2+H2═2NH3,下列说法错误的是( )
| A. | 使用合适的催化剂可以加快反应的速率 | |
| B. | 升高温度可以加快反应速率 | |
| C. | 减小压强能加快反应速率 | |
| D. | 增大N2浓度可以加快反应速率 |
3.下列关于卤族元素的说法中正确的是( )
| A. | 它们单质的熔、沸点随核电荷数的增加逐渐降低 | |
| B. | 元素的非金属性随核电荷数的增加逐渐减小 | |
| C. | 它们原子的氧化性随核电荷数的增加逐渐增强 | |
| D. | 它们氢化物的稳定性随核电荷数的增加逐渐增强 |
2.下列各组物质中,互为同位素的是( )
| A. | 甲烷和乙烷 | B. | 正丁烷和异丁烷 | C. | 金刚石和石墨 | D. | 35Cl 和37Cl |
1.对于${\;}_{19}^{40}$K原子,下列叙述不正确的是( )
| A. | 原子核内质子数为19 | B. | 原子核外电子数为19 | ||
| C. | 质量数为40 | D. | 中子数为40 |
20.密闭容器中可逆反应H2(g)+I2(g)?2HI(g)达到平衡的标志是( )
| A. | H2、I2、HI的浓度相等 | B. | H2、I2、HI的浓度保持不变 | ||
| C. | 混合气体的密度保持不变 | D. | 混合气体的压强不再改变 |
19.若要使0.5mol 甲烷和Cl2发生取代反应,并生成相同物质的量的四种取代物,则需要Cl2的物质的量为
( )
( )
| A. | 2.5 mol | B. | 2 mol | C. | 1.25 mol | D. | 0.5 mol |
18.下列叙述中,不正确的是( )
| A. | 共价化合物中不可能含有离子键 | |
| B. | 硫酸分子中有H+和SO42-两种离子 | |
| C. | 某元素原子的最外层只有一个电子,它跟卤素可能形成离子键,也可能形成共价键 | |
| D. | 离子键和共价键的实质都是电性的相互作用 |
17.在5L的密闭容器中进行下述反应:4NH3+5O2=═4NO+6H20,30S内,NO增加了0.3mol,则在30S内,该反应的平均反应速率正确的是( )
| A. | V(O2 )=0.01mol•L-1•s-1 | B. | V(NO )=0.08mol•L-1•s-1 | ||
| C. | V(H2O)=0.01mol•L-1•s-1 | D. | V(NH3)=0.002mol•L-1•s-1 |
16.下列反应中,属于吸热反应的是( )
| A. | 活泼金属跟酸反应 | B. | 煤气燃烧 | ||
| C. | 酸碱中和反应 | D. | 工业制生石灰 |
15.有机物A为无色粘稠液体,易溶于水.为研究A的组成与结构,进行了如下实验:
0 167525 167533 167539 167543 167549 167551 167555 167561 167563 167569 167575 167579 167581 167585 167591 167593 167599 167603 167605 167609 167611 167615 167617 167619 167620 167621 167623 167624 167625 167627 167629 167633 167635 167639 167641 167645 167651 167653 167659 167663 167665 167669 167675 167681 167683 167689 167693 167695 167701 167705 167711 167719 203614
| 实 验 步 骤 | 解 释 或 实 验 结 论 |
| (1)称取A 9.0g,升温使其汽化,测其密度是相同条件下H2的45倍. | 试通过计算填空: (1)A的相对分子质量为:90. |
| (2)将此9.0gA在足量纯O2充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重5.4g和13.2g. | (2)A的分子式为:C3H6O3. |
| (3)另取A 9.0g,跟足量的NaHCO3粉末反应,生成2.24LCO2(标准状况),若与足量金属钠反应则生成2.24LH2(标准状况). | (3)用结构简式表示A中含有的官能团: -COOH、-OH. |
(4)A的核磁共振氢谱如下图: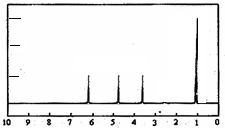 | (4)A中含有4种氢原子. |
(5)综上所述,A的结构简式  . . | |