题目内容
4.对于工业合成氨反应:N2+H2═2NH3,下列说法错误的是( )| A. | 使用合适的催化剂可以加快反应的速率 | |
| B. | 升高温度可以加快反应速率 | |
| C. | 减小压强能加快反应速率 | |
| D. | 增大N2浓度可以加快反应速率 |
分析 A、催化剂可以加快化学反应速率;
B、升高温度可以增大反应速率;
C、压强减小可以减慢化学反应速率;
D、增大物质的浓度可以加快化学反应速率.
解答 解:A.催化剂可降低反应物的活化能,提高活化分子百分数,提高反应速率,故A正确;
B.升高温度可提高活化分子的百分数,提高反应速率,故B正确;
C.减小压强相当于增大体积,单位体积活化分子的数目减小,反应速率也减小,故C错误;
D.增大N2浓度,单位体积活化分子的数目增大,反应速率增大,故D正确.
故选:C.
点评 本题考查学生影响化学反应速率的因素:温度、浓度、压强、催化剂,注意知识的梳理和归纳是前提,难度不大.

练习册系列答案
 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案
相关题目
15.下列根据元素周期表和元素周期律得出的推断中正确的是( )
| A. | 金属元素原子最外层电子数越少,该金属失电子能力越强 | |
| B. | 若存在简单阴离子R2-,则R一定位于ⅥA族 | |
| C. | aA2+、bB+、cC3-三种离子具有相同的电子层结构,则原子序数c>a>b | |
| D. | 铅位于周期表中金属和非金属的交界处,可作半导体材料 |
12.某有机物中有一个C6H5-,一个-CH2-,一个-C6H4-,一个-OH,则该有机物中能使FeCl3溶液显紫色结构有( )
| A. | 二种 | B. | 三种 | C. | 四种 | D. | 五种 |
19.若要使0.5mol 甲烷和Cl2发生取代反应,并生成相同物质的量的四种取代物,则需要Cl2的物质的量为
( )
( )
| A. | 2.5 mol | B. | 2 mol | C. | 1.25 mol | D. | 0.5 mol |
9.下列关于甲烷性质叙述中不正确的是( )
| A. | 甲烷一种无色无味的气体 | B. | 甲烷性质稳定,不和其它物质反应 | ||
| C. | 甲烷极难溶解于水 | D. | 甲烷密度比空气的密度小 |
16.下列说法正确的是( )
| A. | 饱和一元脂肪卤代烃的相对密度随碳原子的增多而增大 | |
| B. | 在酯化反应中,羧酸脱去羧基中的羟基而醇脱去羟基中的氢生成酯和水 | |
| C. | 苯酚有弱酸性,俗称石炭酸,因此它也是一种羧酸 | |
| D. | 在氧气中燃烧时只生成CO2和H2O的物质一定是烃 |
13.下列物质中,既有离子键,又有共价键的是( )
| A. | H2O | B. | CaCl2 | C. | KOH | D. | Na2O2 |
14.如图是化学实验常用装置之一,若气体从右管进入,可用来收集的气体是( )


| A. | NO | B. | CO | C. | NH3 | D. | SO2 |
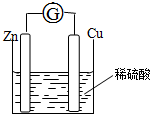 将锌片和铜片用导线相连浸入稀硫酸中组成原电池,两电极间连接一个电流计,装置如图:
将锌片和铜片用导线相连浸入稀硫酸中组成原电池,两电极间连接一个电流计,装置如图: