题目内容
20.密闭容器中可逆反应H2(g)+I2(g)?2HI(g)达到平衡的标志是( )| A. | H2、I2、HI的浓度相等 | B. | H2、I2、HI的浓度保持不变 | ||
| C. | 混合气体的密度保持不变 | D. | 混合气体的压强不再改变 |
分析 根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答 解:A、当体系达平衡状态时,H2、I2、HI的浓度可能相等,也可能不等,与各物质的初始浓度及转化率有关,故A错误;
B、H2、I2、HI的浓度保持不变,说明达平衡状态,故B正确;
C、混合气体的密度一直保持不变,故C错误;
D、气体两边的计量数相等,所以混合气体的压强一直不改变,故D错误;
故选B.
点评 本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.

练习册系列答案
 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案
相关题目
10.下列说法错误的是( )
| A. | 双原子单质分子中的共价键一定是非极性键 | |
| B. | 在共价化合物中一定含有共价键 | |
| C. | 含有离子键的化合物一定是离子化合物 | |
| D. | 含有共价键的化合物一定是共价化合物 |
8.硝酸被称为“国防工业之母”是因为它是制取炸药的重要原料.下列实验事实与硝酸性质不相对应的一组是( )
| A. | 浓硝酸使紫色石蕊试液先变红后褪色--酸性和强氧化性 | |
| B. | 不能用稀硝酸与锌反应制氢气--强氧化性 | |
| C. | 要用棕色瓶盛装浓硝酸--不稳定性 | |
| D. | 稀硝酸能使滴有酚酞的氢氧化钠溶液红色褪去--强氧化性 |
15.有机物A为无色粘稠液体,易溶于水.为研究A的组成与结构,进行了如下实验:
| 实 验 步 骤 | 解 释 或 实 验 结 论 |
| (1)称取A 9.0g,升温使其汽化,测其密度是相同条件下H2的45倍. | 试通过计算填空: (1)A的相对分子质量为:90. |
| (2)将此9.0gA在足量纯O2充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重5.4g和13.2g. | (2)A的分子式为:C3H6O3. |
| (3)另取A 9.0g,跟足量的NaHCO3粉末反应,生成2.24LCO2(标准状况),若与足量金属钠反应则生成2.24LH2(标准状况). | (3)用结构简式表示A中含有的官能团: -COOH、-OH. |
(4)A的核磁共振氢谱如下图: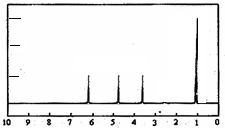 | (4)A中含有4种氢原子. |
(5)综上所述,A的结构简式  . . | |
5.在2L密闭容器中,在一定条件下发生A+3B?2C,在10秒内反应物A的浓度由1mol/L降到0.6mol/L,则ν(A)为( )
| A. | 0.04mol/(L•s) | B. | 0.08mol/(L•s) | C. | 0.4mol/(L•s) | D. | 0.8mol/(L•s) |
12.某有机物的结构简式为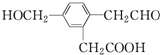 ,它在一定条件下可能发生的反应有( )
,它在一定条件下可能发生的反应有( )
①加成 ②水解 ③酯化 ④氧化 ⑤中和 ⑥消去.
 ,它在一定条件下可能发生的反应有( )
,它在一定条件下可能发生的反应有( )①加成 ②水解 ③酯化 ④氧化 ⑤中和 ⑥消去.
| A. | ②③④ | B. | ①③④⑤⑥ | C. | ①③④⑤ | D. | ①③⑤⑥ |
9.由2-氯丙烷为主要原料制取1,2-丙二醇,经过的反应为( )
| A. | 加成-消去-取代 | B. | 消去-加成-取代 | C. | 取代-消去-加成 | D. | 取代-加成-消去 |
10.有关电解质与非电解质的陈述,合理的是( )
| A. | 在水溶液中能导电的化合物都是电解质 | |
| B. | 在熔融状态下不导电的化合物都是非电解质 | |
| C. | 氨水为混合物,不属于电解质 | |
| D. | 硫酸溶于水能导电,所以浓硫酸为电解质 |
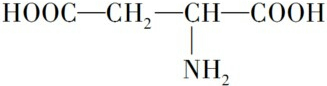 ;B的结构简式为:
;B的结构简式为: .
.