7.不论以何种比例混合,将甲和乙两种混合气体同时通入过量的丙溶液中,一定能产生沉淀的组合是( )
| 序号 | 甲 | 乙 | 丙 |
| ① | CO2 | SO2 | 石灰水 |
| ② | HCl | CO2 | 石灰水 |
| ③ | CO2 | NH3 | Ca(Cl)2 |
| ④ | NO2 | SO2 | BaCl2 |
| ⑤ | CO2 | SO2 | Ba(NO3)2 |
| A. | ②④ | B. | ①②④⑤ | C. | ①③④⑤ | D. | ①②③④ |
6.下列反应所得溶液中一定含有一种溶质的是( )
| A. | 将稀硝酸滴加到装铁粉的试管中 | |
| B. | 向NaOH溶液中通入SO2气体 | |
| C. | 分别将Cl2和SO2通入水中成分反应后的溶液 | |
| D. | 向MgSO4、H2SO4的混合液中加入过量Ba(OH)2溶液 |
4.在一定条件下Na2CO3溶液存在水解平衡:CO32-+H2O?HCO3-+OH-.下列说法正确的是( )
| A. | Na2CO3溶液:c(Na+)>c(CO32-)>c(OH-)>c(H+) | |
| B. | 升高温度,溶液pH减小 | |
| C. | 稀释溶液,溶液中所有离子浓度都减小 | |
| D. | 加入Ba(OH)2固体c(CO32-)增大 |
3.分子式为C3H7OCl,且分子含有烃基的同分异构体的数目为(不考虑立体异构)( )
| A. | 3 | B. | 4 | C. | 5 | D. | 6 |
2.参照反应Br+H?HBr+H的能量对反应历程的示意图,下列叙述中正确的是( )
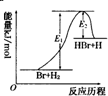

| A. | 该反应的反应热△H=E2-E1 | |
| B. | 加入催化剂,该化学反应的反应热和平衡常数变大 | |
| C. | 正反应的吸热反应 | |
| D. | 升高温度可增大正反应速率,降低逆反应速率 |
20. “神十”宇航员使用的氧气瓶是以聚酯玻璃钢为原料.甲、乙、丙三种物质是合成聚酯玻璃钢的基本原料.下列说法错误的是( )
“神十”宇航员使用的氧气瓶是以聚酯玻璃钢为原料.甲、乙、丙三种物质是合成聚酯玻璃钢的基本原料.下列说法错误的是( )
 “神十”宇航员使用的氧气瓶是以聚酯玻璃钢为原料.甲、乙、丙三种物质是合成聚酯玻璃钢的基本原料.下列说法错误的是( )
“神十”宇航员使用的氧气瓶是以聚酯玻璃钢为原料.甲、乙、丙三种物质是合成聚酯玻璃钢的基本原料.下列说法错误的是( )| A. | 甲物质在一定条件下可以生成有机高分子化合物 | |
| B. | 1mol乙物质可与2mol钠完全反应生成1mol氢气 | |
| C. | 甲、丙物质都能使溴的四氯化碳溶液褪色 | |
| D. | 甲在酸性条件下水解产物之一与乙互为同系物 |
19.能够鉴定溴乙烷中溴元素的存在的操作是( )
0 167481 167489 167495 167499 167505 167507 167511 167517 167519 167525 167531 167535 167537 167541 167547 167549 167555 167559 167561 167565 167567 167571 167573 167575 167576 167577 167579 167580 167581 167583 167585 167589 167591 167595 167597 167601 167607 167609 167615 167619 167621 167625 167631 167637 167639 167645 167649 167651 167657 167661 167667 167675 203614
| A. | 在溴乙烷中直接加入AgNO3溶液 | |
| B. | 在溴乙烷中加蒸馏水,然后加入AgNO3溶液 | |
| C. | 在溴乙烷中加入NaOH溶液,加热后酸化,然后加入AgNO3溶液 | |
| D. | 在溴乙烷中加入乙醇加热后,然后加入AgNO3溶液 |
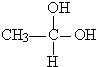 →CH3-CHO+H2O
→CH3-CHO+H2O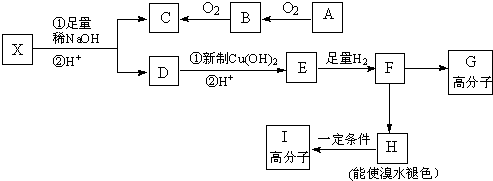
 ;
; ;
; ;
;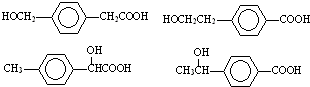 .
.