��Ŀ����
8����1����1.8g̼����2.24L����״����O2�г��ȼ�գ���ȫ����Ӧ��ľ�����÷ų�����30.65kJ����֪��C��s��+O2��g��=CO2��g����H=-393.0kJ•mol-1�ۺ�������Ϣ����д��CO��ȫȼ�յ��Ȼ�ѧ����ʽ2CO��g��+O2��g��=2CO2��g����H=-566KJ/mol����2��������COCl2����һ����Ҫ�Ļ���ԭ�ϣ�����ũҩ��ҽҩ����������ϵ���������ҵ��ͨ��Cl2��g��+CO��g��?COCl2��g����H��0�Ʊ�����ͼ1Ϊij��ģ��ʵ���о��������ݻ�Ϊ1L���ܱ������ڸ����ʵ�Ũ����ʱ��仯�����ߣ��ش��������⣺
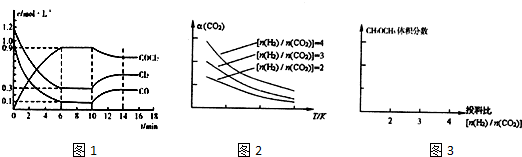
���������¶Ȳ��䣬�ڵ�8min������ϵ�е��������ʸ�1mol����ƽ����Ӧ�������ƶ������Ӧ�����������淴Ӧ����������
��������ʼͶ��Ũ�ȱ�Ϊc��Cl2��=0.8mol/L��c��CO��=0.6mol/L��c��COCl2��=0.4mol/L�����ַ�Ӧ�¶Ȳ��������մﵽ��ѧƽ��ʱ��Cl2�����������������6minʱCl2�����������ͬ��
�۱Ƚϵ�8�뷴Ӧ�¶�T��8�����15min��Ӧ�¶�T��15���ĸߵͣ�T��8����T��15���������������������=����
��3����ȼú�����е�CO2ת��Ϊ�����ѵķ�Ӧԭ��Ϊ��
2CO2��g��+6H2��g��$\stackrel{����}{?}$CH3OCH3��g��+3H2O��g����
����֪һ�������£��÷�Ӧ��CO2��ƽ��ת�������¶ȡ�Ͷ�ϱ�[$\frac{n��{H}_{2}��}{n��C{0}_{2}��}$]�ı仯������ͼ2����������������ʱ������ͼ3�л���ƽ��ʱCH3OCH3�����������Ͷ�ϱ�[$\frac{n��{H}_{2}��}{n��C{0}_{2}��}$]�仯������ͼ��
�ڶ����ѣ�CH3OCH3��ȼ�ϵ�ؿ����������������ʣ����������Խ���ȼ�ϵ�صĸ�����ӦʽΪCH3OCH3-12e-+3H2O=2CO2+12H+��
��4�������½�amol•L-1�Ĵ�����bmol•L-1Ba��OH��2��Һ�������ϣ���ַ�Ӧ����Һ�д���2c��Ba2+��=c��CH3COO-����������Һ�д���ĵ��볣��Ka=$\frac{2b}{a-2b}$��10-7�� ��a��b�Ĵ���ʽ��ʾ��
���� ��1��n��C��=$\frac{1.8g}{12g/mol}$=0.15mol��n��O2��=$\frac{2.24L}{22.4mol/L}$=0.1mol����Ϸ�ӦC+O2=CO2��2C+O2=2CO������ϵ�����жϷ�Ӧ���ɵIJ��n��C����n��O2��=0.15��0.1=3��2��������������ΪCO��CO2�Ļ�����壬̼������ȫ����Ӧ������ֱƽ��д����Ӧ���Ȼ�ѧ����ʽΪ��3C��s��+2O2��g��=2CO��g��+CO2��g����1.8gľ̿����2.24L����״���������г��ȼ�գ�����Ӧ��ľ�����÷ų�����30.65kJ��3molCȫ����Ӧ����30.65KJ/mol��20=613KJ/mol��
3C��s��+2O2��g��=2CO��g��+CO2��g����H=-30.65KJ/mol��20=613KJ/mol��
����C��s��+O2��g��=CO2��g����H=-393.0kJ��mol-1����ϸ�˹���ɼ���õ�CO��ȫȼ�����ɶ�����̼���Ȼ�ѧ����ʽ��
��2���ٸ���ƽ�ⳣ����Ũ�����ж�ƽ���ƶ���
�ڸ������մﵽ��ѧƽ��ʱ��Cl2�����������������6minʱCl2�����������ͬ���뿪ʼƽ��Ϊ��Чƽ�⣬��Ϻ��º�ѹ����Cl2��g��+CO��g��?COCl2��g��ת����һ��һģһ����Ч�����㣻
�۸���ͼ��8min��Ӧ����ƽ��״̬���ڵ�10����ʱ�Ǹı��¶�ʹƽ�����淴Ӧ�����ƶ����������ƽ�����淴Ӧ�����ƶ����жϣ�
��3���ٸ��ݻ�ѧ����ʽ��ϵ�����лش𣻸����¶Ⱥ�ѹǿ�Ի�ѧƽ�ⳣ����Ӱ�죺���ȷ�Ӧ�������¶ȣ�K��С����֮K�������ȷ�Ӧ�������¶ȣ�K����֮K��С��
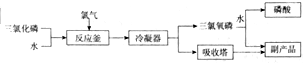
��ԭ��ظ�������������Ӧ���������ڸ����ŵ磬�������������ɶ�����̼���ݴ˽�ɣ�
��4����Һ������������Ũ�ȼ���һ�룬�������ƽ�ⳣ����Ũ���أ���ϸ�����㣬ͨ��״���£���a mol/L�Ĵ�����b mol/L Ba��OH��2��Һ�������ϣ���Һ������Ϊ���ᱵ��������������Ӧƽ��ʱ��2c��Ba2+��=c��CH3COO-��=bmol/L����Һ��c��H+��=c��OH-��=10-7mol/L����Һ�����ԣ��������ƽ�ⳣ�����ݵ��뷽��ʽд��K��
��� �⣺��1��n��C��=$\frac{1.8g}{12g/mol}$=0.15mol��n��O2��=$\frac{2.24L}{22.4mol/L}$=0.1mol����Ϸ�ӦC+O2=CO2��2C+O2=2CO������ϵ�����жϷ�Ӧ���ɵIJ��n��C����n��O2��=0.15��0.1=3��2��������������ΪCO��CO2�Ļ�����壬̼������ȫ����Ӧ��1.8gľ̿����2.24L����״���������г��ȼ�գ�����Ӧ��ľ�����÷ų�����30.65kJ��3molCȫ����Ӧ����30.65KJ/mol��20=613KJ/mol��
��Ӧ���Ȼ�ѧ����ʽΪ��
��3C��s��+2O2��g��=2CO��g��+CO2��g����H=-613KJ/mol
��C��s��+O2��g��=CO2��g����H=-392.0kJ��mol-1��
��ϸ�˹���ɼ��㣬�ڡ�3-�ٵõ�CO��ȫȼ�����ɶ�����̼���Ȼ�ѧ����ʽ��
2CO��g��+O2��g��=2CO2��g����H=-566KJ/mol��
�ʴ�Ϊ��2CO��g��+O2��g��=2CO2��g����H=-566KJ/mol��
��2����8minʱ��ƽ��ʱc��Cl2��=0.3mol/L��c��CO��=0.1mol/L��c��COCl2��=0.9mol/L��
��K=$\frac{0.9}{0.3��0.1}$=30���������Ϊ1L���ڵ�8min�ټ�����ϵ�е��������ʸ�1mol��Qc=$\frac{0.9+1}{��0.3+1������0.1+1��}$=1.33��K������ƽ��������Ӧ�����ƶ����ʴ�Ϊ����Ӧ������
����Ϊ���մﵽ��ѧƽ��ʱ��Cl2�����������������6minʱCl2�����������ͬ���뿪ʼƽ��Ϊ��Чƽ�⣬�ֶ���Cl2��g��+CO��g��?COCl2��g�����º�ѹת����һ��һģһ���ŵ�Ч��������Cl2��g��+CO��g��?COCl2��g��
״̬1 1.2 1.0 0
״̬2 0.8 0.6 c
���մﵽ��ѧƽ��ʱ��״̬2Cl2�����������״̬1 ��6minʱCl2�����������ͬ������c=0.4mol/L���ʴ�Ϊ��0.4��
�۸���ͼ��8min��Ӧ����ƽ��״̬���ڵ�10����ʱ�Ǹı��¶�ʹƽ�����淴Ӧ�����ƶ������ɢ�����ƽ�����淴Ӧ�����ƶ�������T��8����T��15����
�ʴ�Ϊ������
��3����CH3OCH3�����������Ͷ�ϱ�[n��H2��/n��CO2��]������������ݷ�Ӧ֪�����������3��ʱ���ѵ���������������ͼ��ʾ�� ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
��ԭ��ظ�������������Ӧ���������ڸ����ŵ磬�������������ɶ�����̼���缫��ӦʽΪ��CH3OCH3-12e-+3H2O=2CO2+12H+��
�ʴ�Ϊ��CH3OCH3-12e-+3H2O=2CO2+12H+��
��4��ͨ��״���£���a mol/L�Ĵ�����b mol/L Ba��OH��2��Һ�������ϣ���Һ������Ϊ���ᱵ��������������Ӧƽ��ʱ��2c��Ba2+��=c��CH3COO-��=bmol/L����Һ��c��H+��=c��OH-��=10-7mol/L����Һ�����ԣ��������ƽ�ⳣ�����ݵ��뷽��ʽд��K=$\frac{c��C{H}_{3}CO{O}^{-}��c��{H}^{+}��}{c��C{H}_{3}COOH��}$=$\frac{b��1{0}^{-7}}{\frac{a}{2}-b}$=$\frac{2b}{a-2b}$��10-7��
�ú�a��b�Ĵ���ʽ��ʾ�û����Һ�д���ĵ��볣��Ϊ$\frac{2b}{a-2b}$��10-7��
�ʴ�Ϊ��$\frac{2b}{a-2b}$��10-7��
���� �����漰��ѧ����ʽ���Ȼ�ѧ����ʽ����д�ͻ�ѧƽ��ͼ����йؼ��㣬���ڿ��鿼���Է�Ӧ�ȡ���ѧƽ��Ȼ�ѧ��Ӧԭ�����յ�������Ѷ��еȣ�

 ������״Ԫ��ҵϵ�д�
������״Ԫ��ҵϵ�д� ��ʱ�ƿ�������ϰϵ�д�
��ʱ�ƿ�������ϰϵ�д� һ��һ��һ��ͨϵ�д�
һ��һ��һ��ͨϵ�д� �㽭֮��ѧҵˮƽ����ϵ�д�
�㽭֮��ѧҵˮƽ����ϵ�д�| A�� |  ����Һ����������Ũ�����ᾧ | |
| B�� |  �Լ�ϩΪ��ȡ����ȡ��ˮ�е��嵥�� | |
| C�� | 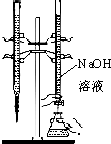 ����֪Ũ�ȵ�����������Һ�ζ�δ֪Ũ�ȵ����� | |
| D�� | 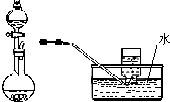 ��ϡ������ͭ��Ӧ��ȡ���ռ�NO |
| A�� | Aԭ�ӵ�������������Bԭ�ӵ������������� | |
| B�� | Aԭ�ӵĵ��Ӳ�����Bԭ�ӵĵ��Ӳ����� | |
| C�� | 1mol A��ϡ�������û���������1mol B�û��������� | |
| D�� | �����£�A�ܴ���ˮ���û�����������B���� |
| A�� | NaCl | B�� | KCl | C�� | CaO | D�� | MgO |
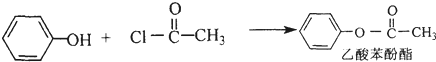 +HCl
+HCl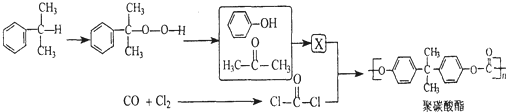
 ��
�� ��
�� ��
��

 ijͬѧΪ̽��Ԫ�����ڱ���Ԫ�����ʵĵݱ���ɣ����������ϵ��ʵ�飮
ijͬѧΪ̽��Ԫ�����ڱ���Ԫ�����ʵĵݱ���ɣ����������ϵ��ʵ�飮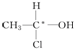 �ȣ����л������д��ڶ�ӳ�칹����ǣ�������
�ȣ����л������д��ڶ�ӳ�칹����ǣ�������