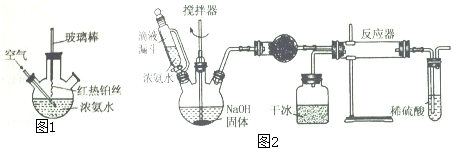
8.利用下列实验装置图可以达到实验目的是( )
| A. | 此装置可以实现Cl2的制取、收集、尾气吸收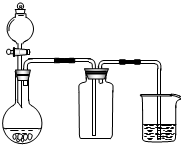 | |
| B. | 此装置可以实现乙酸乙酯的制取和收集 | |
| C. | 此装置可以形成Cu-Zn原电池 | |
| D. | 此装置可证明H2CO3酸性大于H2SiO3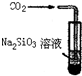 |
7.下列有关对定量实验误差分析正确的是( )
| A. | 中和热测定实验中,缓慢地将NaOH溶液倒入测定装置中--测定结果无影响 | |
| B. | 酸碱中和滴定实验中,滴定前无气泡而滴定后有气泡_测定结果偏高 | |
| C. | 测定溶液pH的实验中,用干燥pH试纸测定新制氯水的pH--测定结果无影响 | |
| D. | 现需90mL 1.0mol•L-1NaOH溶液,称取3.6gNaOH固体配制--溶液浓度偏低 |
6.工业上由焦炭或夭然气制氢气的过程中会产生一氧化碳.为了除去氢气中混有的一氧化碳,可在催化剂存在的条件下将一氧化碳与水蒸气发生反应:CO(g)+H2O( g)?CO2(g)+H2(g)△H=-41.0kJ•mol-l.该反应在工业上被称为“一氧化碳变换”.
(1)写出该反应的平衡常数表达式:K=$\frac{c(C{O}_{2})×c({H}_{2})}{c(CO)×c({H}_{2}O)}$; K( 200℃)> K( 300℃)(填“>”、“=”或“<”).
(2)在773K时,一氧化碳变换反应的平衡常数K=9,如反应开始时CO和H2O的浓度都是0.020•mol-l,则在此反应条件下一氧化碳的转化率为75%.
(3)某工业合成氨的原料气组成为:H2 40%、N2 20%、CO30%、CO210%(均为体积分数).现采用“一氧化碳变换”法,向上述原料气中加入水蒸气,以除去其中的CO.已知不同温度及反应物投料比($\frac{n{H}_{2}O}{n(CO)}$ )下,变换后平衡混合气体中CO的体积分数如下表所示:
①从表中数据可以得到控制不同条件时CO的转化率的变化规律.能使CO的转化率升高,可改变的条件降低温度、增大反应物投料比($\frac{n{H}_{2}O}{n(CO)}$ )或原料气中水蒸气的比例.
②温度是一氧化碳变换工艺中最重要的工艺条件,实际生产过程中将温度控制在300℃左右,其原因是提高温度,会提高反应速率,但平衡逆向移动,CO的转化率下降,实际生产过程中应该综合考虑速率和平衡两个方面.
③温度为300℃、$\frac{n{H}_{2}O}{n(CO)}$=1时,变换后的平衡混合气体中CO2的体积分数是24.8%.(结果保留3位有效数字).
0 166962 166970 166976 166980 166986 166988 166992 166998 167000 167006 167012 167016 167018 167022 167028 167030 167036 167040 167042 167046 167048 167052 167054 167056 167057 167058 167060 167061 167062 167064 167066 167070 167072 167076 167078 167082 167088 167090 167096 167100 167102 167106 167112 167118 167120 167126 167130 167132 167138 167142 167148 167156 203614
(1)写出该反应的平衡常数表达式:K=$\frac{c(C{O}_{2})×c({H}_{2})}{c(CO)×c({H}_{2}O)}$; K( 200℃)> K( 300℃)(填“>”、“=”或“<”).
(2)在773K时,一氧化碳变换反应的平衡常数K=9,如反应开始时CO和H2O的浓度都是0.020•mol-l,则在此反应条件下一氧化碳的转化率为75%.
(3)某工业合成氨的原料气组成为:H2 40%、N2 20%、CO30%、CO210%(均为体积分数).现采用“一氧化碳变换”法,向上述原料气中加入水蒸气,以除去其中的CO.已知不同温度及反应物投料比($\frac{n{H}_{2}O}{n(CO)}$ )下,变换后平衡混合气体中CO的体积分数如下表所示:
| 投料比 CO体积分数/% 温度/℃ | $\frac{n{H}_{2}O}{n(CO)}$=1 | $\frac{n{H}_{2}O}{n(CO)}$=3 | $\frac{n{H}_{2}O}{n(CO)}$=5 |
| 200 250 300 350 | 1.70 2.73 6.00 7.85 | 0.21 0.30 0.84 1.52 | 0.02 0.06 0.43 0.80 |
②温度是一氧化碳变换工艺中最重要的工艺条件,实际生产过程中将温度控制在300℃左右,其原因是提高温度,会提高反应速率,但平衡逆向移动,CO的转化率下降,实际生产过程中应该综合考虑速率和平衡两个方面.
③温度为300℃、$\frac{n{H}_{2}O}{n(CO)}$=1时,变换后的平衡混合气体中CO2的体积分数是24.8%.(结果保留3位有效数字).
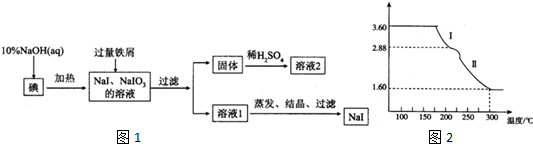
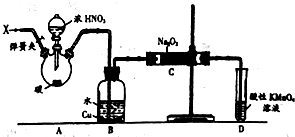 亚硝酸钠(NaNO2)被称为工业盐,在漂白、电镀等方面应用广泛.以木炭、浓硝酸、水和铜为原料制备硝酸钠的装置如图所示.
亚硝酸钠(NaNO2)被称为工业盐,在漂白、电镀等方面应用广泛.以木炭、浓硝酸、水和铜为原料制备硝酸钠的装置如图所示. 随着我国工业化水平的不断发展,解决水、空气污染问题成为重要课题.
随着我国工业化水平的不断发展,解决水、空气污染问题成为重要课题.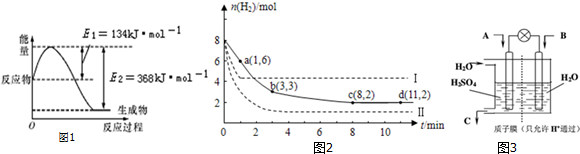

 在分析化学中常用Na2C2O4晶体(溶液无色)作为基准物质测定KMnO4溶液的浓度.在H2SO4溶液中,反应如下:2MnO${\;}_{4}^{-}$+5C2O${\;}_{4}^{2-}$+16H+$\frac{\underline{\;75℃-85℃\;}}{\;}$2Mn2+(溶液无色)+10CO2↑+8H2O.
在分析化学中常用Na2C2O4晶体(溶液无色)作为基准物质测定KMnO4溶液的浓度.在H2SO4溶液中,反应如下:2MnO${\;}_{4}^{-}$+5C2O${\;}_{4}^{2-}$+16H+$\frac{\underline{\;75℃-85℃\;}}{\;}$2Mn2+(溶液无色)+10CO2↑+8H2O.