题目内容
7.下列有关对定量实验误差分析正确的是( )| A. | 中和热测定实验中,缓慢地将NaOH溶液倒入测定装置中--测定结果无影响 | |
| B. | 酸碱中和滴定实验中,滴定前无气泡而滴定后有气泡_测定结果偏高 | |
| C. | 测定溶液pH的实验中,用干燥pH试纸测定新制氯水的pH--测定结果无影响 | |
| D. | 现需90mL 1.0mol•L-1NaOH溶液,称取3.6gNaOH固体配制--溶液浓度偏低 |
分析 A.缓慢地将NaOH溶液倒入测定装置中,会使热量损失;
B.根据c(待测)=$\frac{C(标准)×V(标准)}{V(待测)}$分析;
C.新制氯水中含有次氯酸,能漂白pH试纸;
D.配制90mL 1.0mol•L-1NaOH溶液,需要选用100mL容量瓶,根据100mL 1.0mol•L-1NaOH溶液中氢氧化钠的物质的量计算出氢氧化钠的质量;
解答 解:A.缓慢地将NaOH溶液倒入测定装置中,会使热量损失,造成中和热测量数值偏小,故A不选;
B.滴定前无气泡而滴定后有气泡,造成V(标准)偏小,根据c(待测)=$\frac{C(标准)×V(标准)}{V(待测)}$分析,测定结果偏小,故B不选;
C.新制氯水中含有次氯酸,能漂白pH试纸,不可用pH试纸测定新制氯水的pH,故C不选;
D.实验室没有90mL容量瓶,配制90mL 1.0mol•L-1NaOH溶液,需要选用100mL容量瓶,需要氢氧化钠的物质的量为:1mol/L×0.10L=0.1mol,需要氢氧化钠的质量为:40g/mol×0.1mol=4.0g,称取3.6gNaOH固体配制,溶质偏小,溶液浓度偏低,故D选.
故选D.
点评 本题考查了中学化学常见的实验操作注意事项,掌握操作原理和注意事项即可,注意容量瓶只能配制与其规格一致体积的溶液,难度中等.

练习册系列答案
 全能测控一本好卷系列答案
全能测控一本好卷系列答案
相关题目
10.下列叙述中,正确的是( )
| A. | 不同的原子之间只能构成共价化合物 | |
| B. | 单质中不一定存在非极性键 | |
| C. | 非金属原子之间只能构成共价化合物 | |
| D. | Cl2的沸点比F2高,这与化学建的大小有关 |
19.下列关于热化学反应的描述中正确的是( )
| A. | 一定条件下,将0.5 mol N2和1.5 mol H2置于密闭容器中充分反应生成NH3放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)=2NH3(g)△H=-38.6 kJ•mol-1 | |||||||||||
| B. | CO(g)的燃烧热是283.0kJ/mol,则2CO2(g)=2CO(g)+O2(g);△H=+566.0kJ/mol
| |||||||||||
| C. | 已知则可以计算CH3-CH3(g)→CH2=CH2(g)+H2(g);△H=+125.6 kJ/mol | |||||||||||
| D. | 同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的△H不同 |
16.根据下列热化学方程式,判断氢化物的稳定性顺序正确的是( )
N2(g)+3H2 (g)=2NH3(g)△H=-92.38kJ•mol-1
H2(g)+Cl2(g)=2HCl(g)△H=-184.72kJ•mol-1
I2(g)+H2(g)=2HI(g)△H=+51.92kJ•mol-1.
N2(g)+3H2 (g)=2NH3(g)△H=-92.38kJ•mol-1
H2(g)+Cl2(g)=2HCl(g)△H=-184.72kJ•mol-1
I2(g)+H2(g)=2HI(g)△H=+51.92kJ•mol-1.
| A. | HI>HCl>NH3 | B. | HCl>NH3>HI | C. | HCl>HI>NH3 | D. | NH3>HI>HCl |
 .
. 
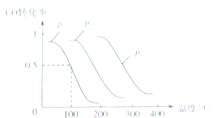 我国煤炭资源比石油和天然气资源丰富,煤的综合利用主要是指煤的气化和液化.回答下列问题:
我国煤炭资源比石油和天然气资源丰富,煤的综合利用主要是指煤的气化和液化.回答下列问题: