题目内容
10.下表是元素周期表的一部分,针对表中的①~⑦种元素,填写下列空白:| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ |
(2)这些元素的最高价氧化物的对应水化物中,酸性最强的化合物的分子式是HClO4;碱性最强的化合物的电子式是
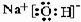 ;能形成两性氢氧化物的元素是Al.
;能形成两性氢氧化物的元素是Al.(3)②的氢化物分子式为NH3,属于共价化合物(填“共价”或“离子”);
(4)⑤元素的原子结构示意图为
 .
.
分析 由元素在周期表中的位置可知①~⑦分别为C、N、Na、Al、S、Cl、Ar等元素,
(1)根据同周期自左而右金属性减弱、非金属性增强,同主族自上而下金属性增强、非金属性减弱稀有气体原子最外层为稳定结构;
(2)这几种元素中,非金属性最强的是Cl元素,金属性最强的金属是Na,呈两性的氢氧化物是Al(OH)3;
(3)②为N元素,对应的氢化物为NH3,属于共价化合物;
(4)⑤为S元素,原子核外有3的电子层,最外层电子数为6.
解答 解:由元素在周期表中的位置可知①~⑦分别为C、N、Na、Al、S、Cl、Ar等元素,
(1)根据同周期自左而右金属性减弱、非金属性增强,同主族自上而下金属性增强、非金属性减弱,故表中金属性最强为Na,非金属性最强的为Cl,稀有气体原子最外层为稳定结构,化学性质最不活泼为Ar,
故答案为:Na; Cl;Ar;
(2)这几种元素中,非金属性最强的是Cl元素,则酸性最强的酸是HClO4,金属性最强的金属是Na,所以NaOH的碱性最强,电子式为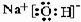 ,呈两性的氢氧化物是Al(OH)3,
,呈两性的氢氧化物是Al(OH)3,
故答案为:HClO4;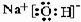 ;Al;
;Al;
(3)②为N元素,对应的氢化物为NH3,属于共价化合物,故答案为:NH3;共价;
(4)⑤为S元素,原子核外有3的电子层,最外层电子数为6,对应的原子结构示意图为 ,故答案为:
,故答案为: ;
;
点评 本题考查了元素周期表和元素周期律综合应用,涉及化学基本用语、元素周期率等知识点,根据物质结构、元素周期律等知识点分析解答即可,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
18.化学与生产、生活、社会密切相关,下列说法错误的是( )
| A. | 葡萄糖、麦芽糖均能与新制Cu(OH)2反应 | |
| B. | 富含蛋白质的豆浆煮沸后即可得人体所需的氨基酸 | |
| C. | 当人误食重金属盐时,可喝大量的牛奶、蛋清解毒 | |
| D. | 油脂在氢氧化钾溶液中水解可制得汽车洗涤用的液体肥皂 |
15.某元素R的最高价氧化物的化学式为RO2,且R的气态氢化物中氢的质量分数为25%,此元素是( )
| A. | C | B. | N | C. | Si | D. | P |
2.2015年6月5日是世界环境日,今年的主题是“践行绿色生活,”下列有关说法中错误的是( )
| A. | 煤的气化、液化是使煤变成清洁能源,减少环境污染的有效途径 | |
| B. | 高纯硅可制作太阳能电池,二氧化硅可制作光导纤维 | |
| C. | 利用工业生产产生的二氧化碳制造全降解塑料,可以缓解温室效应 | |
| D. | 棉、麻、羊毛及合成纤维完全燃烧都只生成CO2和H2O |
19.用惰性电极电解下列溶液的说法正确是( )
| A. | 电解氯化钾溶液的过程中,溶液的pH变小 | |
| B. | 电解硝酸银溶液的过程中,阴极质量不变,阳极质量增大 | |
| C. | 电解硫酸钠溶液的过程中,两极产生气体的物质的量不相同 | |
| D. | 电解氢氧化钠溶液的过程中,氢氧化钠的物质的量浓度减小 |
 .
. .
. .
. .
.
 ;
; ,形成该化合物的化学键有离子键和共价键
,形成该化合物的化学键有离子键和共价键