题目内容
18.化学与生产、生活、社会密切相关,下列说法错误的是( )| A. | 葡萄糖、麦芽糖均能与新制Cu(OH)2反应 | |
| B. | 富含蛋白质的豆浆煮沸后即可得人体所需的氨基酸 | |
| C. | 当人误食重金属盐时,可喝大量的牛奶、蛋清解毒 | |
| D. | 油脂在氢氧化钾溶液中水解可制得汽车洗涤用的液体肥皂 |
分析 A、葡萄糖和麦芽糖均为还原性糖;
B、蛋白质煮沸时不能水解;
C、可溶性重金属盐能使蛋白质变性;
D、汽车洗涤用的液体肥皂的主要成分为硬脂酸钾.
解答 解:A、葡萄糖和麦芽糖均为还原性糖,均含醛基,故均能与新制的氢氧化铜反应生成砖红色沉淀,故A正确;
B、蛋白质煮沸时不能水解为氨基酸,只有在人体内在蛋白酶的作用下才能水解为人体需要的氨基酸,故B错误;
C、可溶性重金属盐能使蛋白质变性,故能使人中毒,而当人误食重金属盐时,可喝大量的牛奶、蛋清等富含蛋白质的物质来替代人体中毒,从而缓解人体解毒,故C正确;
D、汽车洗涤用的液体肥皂的主要成分为硬脂酸钾,是用油脂在KOH溶液中水解制得的,故D正确.
故选B.
点评 本题考查了化学在生活中的应用,应注意的是可溶性重金属盐能使蛋白质变性,即氯化钡能使人中毒,但BaSO4无毒.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
14.将锌片和铜片用导线连接置于同一稀硫酸中组成原电池,下列叙述不正确的是( )
| A. | 锌片发生氧化反应 | B. | 铜片发生还原反应 | ||
| C. | 铜片上有氢气析出 | D. | 电子从锌片流出,流向铜片 |
9.在下列各指定溶液中,离子可能大量共存的是( )
| A. | 澄清透明的溶液中:Cu2+、Fe3+、NO3-、Cl- | |
| B. | 使pH试纸变蓝的溶液中:NH4+、Na+、SO42-、Cl- | |
| C. | 含有大量ClO-的溶液中:K+、OH-、I-、SO32- | |
| D. | c(Fe3+)=0.1mol•L-1的溶液中:K+、ClO-、SO42-、SCN- |
3.根据表中信息判断,下列选项正确的是( )
| 序号 | 反应物 | 产物 |
| ① | KMnO4、H2O2、H2SO4 | K2SO4、MnSO4… |
| ② | MnO4-… | Cl2、Mn2+… |
| ③ | Cl2、FeBr2 | FeCl3、FeBr3 |
| A. | 第①组反应的其余产物为H2O | |
| B. | 第②组反应中生成lmol Cl2,转移电子5mol | |
| C. | 第③组反应中Cl2与FeBr2的物质的量之比小于或等于1:2 | |
| D. | 氧化性由强到弱顺序为MnO4->Cl2>Fe3+>Br2 |
10.下表是元素周期表的一部分,针对表中的①~⑦种元素,填写下列空白:
(1)在这些元素中,(用元素符号填写,下同)金属性最强的元素是Na;非金属性最强的是Cl;最不活泼的元素是Ar.
(2)这些元素的最高价氧化物的对应水化物中,酸性最强的化合物的分子式是HClO4;碱性最强的化合物的电子式是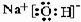 ;能形成两性氢氧化物的元素是Al.
;能形成两性氢氧化物的元素是Al.
(3)②的氢化物分子式为NH3,属于共价化合物(填“共价”或“离子”);
(4)⑤元素的原子结构示意图为 .
.
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ |
(2)这些元素的最高价氧化物的对应水化物中,酸性最强的化合物的分子式是HClO4;碱性最强的化合物的电子式是
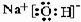 ;能形成两性氢氧化物的元素是Al.
;能形成两性氢氧化物的元素是Al.(3)②的氢化物分子式为NH3,属于共价化合物(填“共价”或“离子”);
(4)⑤元素的原子结构示意图为
 .
.
7.下列各组物质中,互为同系物的是( )
| A. | CH4和CH3CH2CH3 | B. | ${\;}_{17}^{35}$Cl和${\;}_{17}^{37}$Cl | ||
| C. | 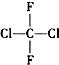 和 和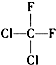 | D. |  和CH3-CH2-CH2-CH3 和CH3-CH2-CH2-CH3 |
8.贵州开磷(集团)有限责任公司按照循环经济的发展理念,将工业合成氨与制备甲醇进行联合生产,现已具备年产60万吨合成氨、38万吨甲醇的生产能力.其生产流程如图1:
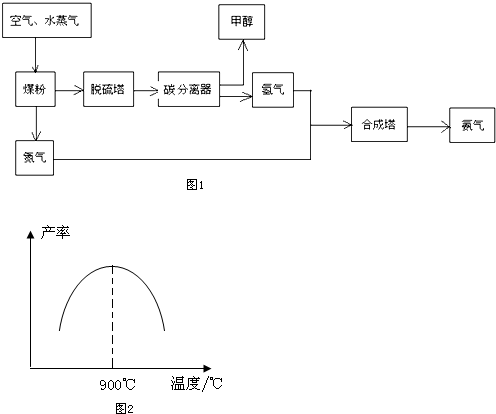
请回答下列问题:
(1)工业生产时,水蒸气可与煤粉反应制备H2,反应的化学方程式为C+H2O(g)$\frac{\underline{\;高温\;}}{\;}$CO+H2;
(2)工业制取氢气的另一个反应为:CO+H2O(g)?CO2+H2.在T℃时,往1L密闭容器中充入0.2molCO和0.3mol水蒸气,反应达平衡后,体系中c(H2)═0.12mol•L-1.该温度下此反应的平衡常数K=1(填计算结果);
(3)若在恒温恒容的容器内进行反应CO(g)+2H2 (g)?C H3OH(g),在密闭容器中开始只加入CO、H2,反应10min后测得各组分的浓度如下:
①该时间段内反应速率v(H2)=0.08mol/(L•min);
②该反应达到平衡状态的标志是BC(填字母序号);
A.有1个H-H键生成的同时有3个C-H键生成
B.CO的百分含量保持不变
C.容器中混合气体的压强不变化
D.容器中混合气体的密度不变化
(4)已知在常温常压下:
①2C H3OH(l)+3O2 (g)?2CO2 (g)+4H2 O(g)△H1=-1275.6kJ/mol
②2C O(l)+O2 (g)?2CO2 (g)△H2=-566.0kJ/mol
③H2O (g)?H2 O(l)△H3=-44.0kJ/mol
写出甲醇不完燃烧生成一氧化碳和液态水的热化学方程式CH3OH(l)+O2(g)=CO(g)+2H2O(l)△H=-442.8kJ•mol-1;
(5)N2和H2以铁作催化剂从145℃就开始反应,不同温度下NH3的产率如图2所示.温度高于900℃时,NH3产率下降的原因是温度高于900℃时,平衡向左移动;生产过程中合成气要进行循环,其目的是提高原料的利用率.

请回答下列问题:
(1)工业生产时,水蒸气可与煤粉反应制备H2,反应的化学方程式为C+H2O(g)$\frac{\underline{\;高温\;}}{\;}$CO+H2;
(2)工业制取氢气的另一个反应为:CO+H2O(g)?CO2+H2.在T℃时,往1L密闭容器中充入0.2molCO和0.3mol水蒸气,反应达平衡后,体系中c(H2)═0.12mol•L-1.该温度下此反应的平衡常数K=1(填计算结果);
(3)若在恒温恒容的容器内进行反应CO(g)+2H2 (g)?C H3OH(g),在密闭容器中开始只加入CO、H2,反应10min后测得各组分的浓度如下:
| 物质 | H2 | CO | C H3OH |
| 浓度/(mol•L-1) | 0.20 | o.10 | o.40 |
②该反应达到平衡状态的标志是BC(填字母序号);
A.有1个H-H键生成的同时有3个C-H键生成
B.CO的百分含量保持不变
C.容器中混合气体的压强不变化
D.容器中混合气体的密度不变化
(4)已知在常温常压下:
①2C H3OH(l)+3O2 (g)?2CO2 (g)+4H2 O(g)△H1=-1275.6kJ/mol
②2C O(l)+O2 (g)?2CO2 (g)△H2=-566.0kJ/mol
③H2O (g)?H2 O(l)△H3=-44.0kJ/mol
写出甲醇不完燃烧生成一氧化碳和液态水的热化学方程式CH3OH(l)+O2(g)=CO(g)+2H2O(l)△H=-442.8kJ•mol-1;
(5)N2和H2以铁作催化剂从145℃就开始反应,不同温度下NH3的产率如图2所示.温度高于900℃时,NH3产率下降的原因是温度高于900℃时,平衡向左移动;生产过程中合成气要进行循环,其目的是提高原料的利用率.