题目内容
14.已知由石墨制备金刚石的反应为:C(石墨)$\frac{\underline{\;一定条件\;}}{\;}$C(金刚石);△H>0,则下列两个反应中:C(石墨)+O2(g)═CO2(g);△H=a kJ/mol,C(金刚石)+O2(g)═CO2(g);△H=b kJ/mol,a与b的关系为( )| A. | a>b | B. | a<b | C. | a=b | D. | 无法确定 |
分析 利用盖斯定律写出金刚石与石墨转化的热化学方程式判断a与b的关系.
解答 解:①C(石墨)+O2(g)═CO2(g);△H=a kJ/mol,
②C(金刚石)+O2(g)═CO2(g);△H=b kJ/mol,
利用盖斯定律将①-②可得:C(石墨)=C(金刚石)△H=(a-b)kJ•mol-1,则a-b>0,即a>b,故选A.
点评 本题考查盖斯定律的应用,题目难度不大,注意盖斯定律的掌握.

练习册系列答案
 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案 小学期末标准试卷系列答案
小学期末标准试卷系列答案
相关题目
20.下列说法正确的是( )
| A. | 同周期主族元素简单离子的半径随核电荷数的增加而减小 | |
| B. | 同主族元素含氧酸的酸性随核电荷数的增加而降低 | |
| C. | 质子数相同的微粒化学性质也相同 | |
| D. | ${\;}_{92}^{235}$U与${\;}_{92}^{238}$U具有相同的核外电子排布 |
9.由短周期前10号元素组成的物质T和X,有如图所示的转化.X不稳定,易分解.为使得下列转化能够成功进行,方框内不可能加入的反应试剂是( )
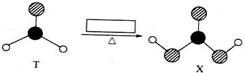

| A. | 新制Cu(OH)2悬浊液 | B. | 溴水 | C. | 酸性KMnO4溶液 | D. | NaOH溶液 |
6.生活中的问题常涉及化学知识,下列过程不涉及化学变化的是( )
| A. | 用食醋除去暖瓶内的水垢 | |
| B. | 鸡蛋白溶液中加入硫酸铵饱和溶液后析出白色沉淀 | |
| C. | 淀粉溶液中加碘水变蓝 | |
| D. | 棉花织品和羊毛织品:分别灼烧闻气味 |
3.下列实验操作中可行的是( )
| A. | 用溴水鉴别苯、四氯化碳、苯乙烯 | |
| B. | 除去苯中少量苯酚,先加浓溴水,再过滤 | |
| C. | 用酸性高锰酸钾溶液洗气,可以除去乙烷气体中乙烯 | |
| D. | 除去乙酸乙酯中的乙酸和乙醇可用氢氧化钠溶液洗涤,再分液 |
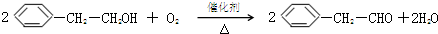 .
. .
.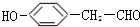 .
.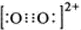 ; O22+中σ键数目和π键数目之比为1:2.
; O22+中σ键数目和π键数目之比为1:2.