题目内容
19.有机物H是一种合成药物的中间体,H的合成方案如下: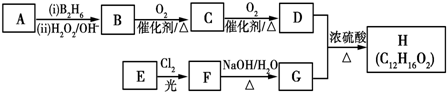
已知:R-CH═CH2$\underset{\stackrel{i.{B}_{2}{H}_{6}}{→}}{ii.{H}_{2}{O}_{2}/O{H}^{-}}$ RCH2CH2OH
请回答下列问题:
(1)A为相对分子质量为104的芳香烃,A的分子式为C8H8.
(2)鉴别A和C两种有机物的试剂为银氨溶液或新制氢氧化铜.
(3)F为一氯代物,其核磁共振氢谱有三个吸收峰,则E的结构简式为(CH3)3CH.
(4)写出B→C的化学方程式:
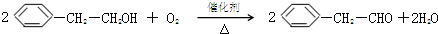 .
.(5)写出D和G生成H的化学方程式:
 .
.(6)D的同分异构体中能与FeCl3溶液发生显色反应且能发生银镜反应的有13种,写出其中核磁共振氢谱中吸收峰数目最少的结构简式
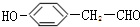 .
.
分析 A是相对分子质量为104的芳香烃,分子中碳原子最大数目为$\frac{104}{12}$=8…8,故A的分子式为C8H8,结构简式为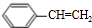 ,A发生信息反应生成B为
,A发生信息反应生成B为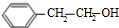 ,B发生氧化反应生成C为
,B发生氧化反应生成C为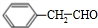 ,C发生氧化反应生成D为
,C发生氧化反应生成D为 .F为一氯代物,水解得到G含有羟基,D与G发生酯化反应生成H,结合D、H的分子式可知G的分子式为C4H10O,F的核磁共振氢谱有三个吸收峰,则F为(CH3)2CHCH2Cl,故G为(CH3)2CHCH2OH,E为(CH3)3CH,据此解答.
.F为一氯代物,水解得到G含有羟基,D与G发生酯化反应生成H,结合D、H的分子式可知G的分子式为C4H10O,F的核磁共振氢谱有三个吸收峰,则F为(CH3)2CHCH2Cl,故G为(CH3)2CHCH2OH,E为(CH3)3CH,据此解答.
解答 解:A是相对分子质量为104的芳香烃,分子中碳原子最大数目为$\frac{104}{12}$=8…8,故A的分子式为C8H8,结构简式为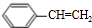 ,A发生信息反应生成B为
,A发生信息反应生成B为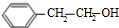 ,B发生氧化反应生成C为
,B发生氧化反应生成C为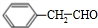 ,C发生氧化反应生成D为
,C发生氧化反应生成D为 .F为一氯代物,水解得到G含有羟基,D与G发生酯化反应生成H,结合D、H的分子式可知G的分子式为C4H10O,F的核磁共振氢谱有三个吸收峰,则F为(CH3)2CHCH2Cl,故G为(CH3)2CHCH2OH,E为(CH3)3CH,
.F为一氯代物,水解得到G含有羟基,D与G发生酯化反应生成H,结合D、H的分子式可知G的分子式为C4H10O,F的核磁共振氢谱有三个吸收峰,则F为(CH3)2CHCH2Cl,故G为(CH3)2CHCH2OH,E为(CH3)3CH,
(1)由上述分析可知,A的分子式为C8H8,故答案为:C8H8;
(2)A为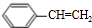 ,含有碳碳双键,C为
,含有碳碳双键,C为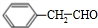 ,含有醛基,用银氨溶液或新制氢氧化铜可以区别二者,故答案为:银氨溶液或新制氢氧化铜;
,含有醛基,用银氨溶液或新制氢氧化铜可以区别二者,故答案为:银氨溶液或新制氢氧化铜;
(3)由上述分析可知,则E的结构简式为(CH3)3CH,故答案为:(CH3)3CH;
(4)B→C的化学方程式为: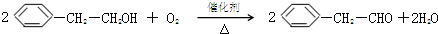 ,
,
故答案为: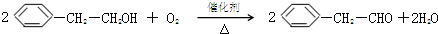 ;
;
(5)D和G生成H的化学方程式为: ,
,
故答案为: ;
;
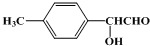
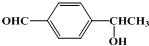
(6)D( )的同分异构体中能与FeCl3溶液发生显色反应且能发生银镜反应,含有酚羟基、醛基,侧链为-OH、-CH2CHO时,有邻、间、对3种位置,侧链为-OH、-CHO、-CH3时,若-OH、-CHO相邻时,-CH3有4种位置,若-OH、-CHO相间时,-CH3有4种位置,若-OH、-CHO相对时,-CH3有2种位置,故符合条件的同分异构体有:3+4+4+2=13种,其中核碰共振氢谱中吸收峰数目最少的结构简式为:
)的同分异构体中能与FeCl3溶液发生显色反应且能发生银镜反应,含有酚羟基、醛基,侧链为-OH、-CH2CHO时,有邻、间、对3种位置,侧链为-OH、-CHO、-CH3时,若-OH、-CHO相邻时,-CH3有4种位置,若-OH、-CHO相间时,-CH3有4种位置,若-OH、-CHO相对时,-CH3有2种位置,故符合条件的同分异构体有:3+4+4+2=13种,其中核碰共振氢谱中吸收峰数目最少的结构简式为: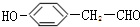 ,故答案为:13;
,故答案为:13;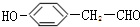 .
.
点评 本题考查有机物推断,根据相对分子质量计算确定A的结构简式是关键,结合反应条件进行推断,再结合D、H的分子式确定G的分子式,需要学生熟练掌握官能团的性质与转化,难度中等.

 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案| A. | 5.6 g铁与足量盐酸反应转移的电子数为0.3NA | |
| B. | 标准状况下,11.2LSO3所含的分子数为0.5NA | |
| C. | 标准状况下,22.4 L氦气与22.4 L氟气所含原子数均为2 NA | |
| D. | 20 g重水(D2O)中含有的电子数为10NA |
| A. | 亚硫酸钡与盐酸反应:BaSO3+2H+=Ba2++SO2↑+H2O | |
| B. | 少量二氧化碳通入足量的NaOH溶液:CO2+OH-=HCO${\;}_{3}^{-}$ | |
| C. | 澄清石灰水跟盐酸反应:H++OH-=H2O | |
| D. | 亚硫酸氢钠溶液与NaOH溶液反应:HSO${\;}_{3}^{-}$+OH-=SO${\;}_{3}^{2-}$+H2O |
| A. | 用溴水可鉴别苯、CCl4、苯乙烯 | |
| B. | 加浓溴水,然后过滤可除去苯中少量苯酚 | |
| C. | 苯、溴水、铁粉混合制成溴苯 | |
| D. | 向液态溴苯中加入硝酸银溶液,观察有无淡黄色沉淀生成,以检验溴元素的存在 |
| A. | a>b | B. | a<b | C. | a=b | D. | 无法确定 |
| A. | 臭氧、乙醇溶液均可用于消毒杀菌且原理完全相同 | |
| B. | 半导体材料和光纤制品都是以硅为基本原料生产的 | |
| C. | 煤的干馏和石油的分馏均属化学变化 | |
| D. | 亚硝酸盐、二氧化硫均可以用作食品的防腐剂 |
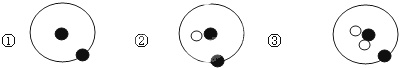
| A. | ①、②、③互为同位素 | B. | ①、②、③互为同素异形体 | ||
| C. | ①、②、③是三种化学性质不同的核素 | D. | ①、②、③质量数相同 |

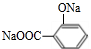 .
.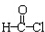 +CH3CH2OH→
+CH3CH2OH→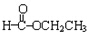 +HCl
+HCl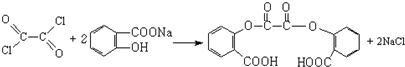
 .
. 、
、 等、
等、