题目内容
10.下列有关叙述正确的是( )| A. | 只含有离子键的化合物才是离子化合物 | |
| B. | 硫酸铵晶体是含有离子键、极性键和配位键的分子晶体 | |
| C. | 由于I-I键的键能比F-F、Cl-Cl、Br-Br键的键能都小,所以在卤素单质中碘的熔点最低 | |
| D. | 在分子晶体中一定不存在离子键,而在离子晶体中可能存在共价键 |
分析 A.离子化合物中一定含离子键;
B.硫酸铵中含有离子键、极性共价键和配位键;
C.分子晶体的熔沸点与相对分子质量成正比;
D.分子晶体中一定不含离子键,含有离子键的晶体属于离子晶体.
解答 解:A.离子化合物中一定含离子键,可能还含共价键,故A错误;
B.硫酸铵中铵根离子和硫酸根离子之间存在离子键,氮原子和氢原子之间存在共价键和配位键,属于离子晶体,故B错误;
C.分子晶体的熔沸点与相对分子质量成正比,碘分子的相对分子质量比氟气、氯气和溴的大,所以其熔沸点最高,故C错误;
D.分子晶体中一定不含离子键,含有离子键的晶体属于离子晶体,离子晶体中可能含有共价键,如NaOH属于离子晶体,含有共价键,故D正确;
故选D.
点评 本题考查化学键与化合物的类型,注意利用实例分析选项,把握特殊物质中的化学键及稀有气体中不含化学键,题目难度不大.

练习册系列答案
 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目
20.几种短周期元素的原子半径及主要化合价如下表:
下列叙述正确的是( )
| 元素代号 | X | Y | Z | W |
| 原子半径/pm | 160 | 143 | 75 | 74 |
| 主要化合价 | +2 | +3 | +5、+3、-3 | -2 |
| A. | X、Y元素的金属性X<Y | |
| B. | 一定条件下,Z单质与W的常见单质直接生成ZW2 | |
| C. | Y的最高价氧化物对应的水化物能溶于稀氨水 | |
| D. | 四种元素形成的单核离子半径由大到小的顺序为:Z3->W2->X2+>Y3+ |
18.下列物质在固态时,晶体类型相同的是( )
| A. | SiO2和CO2 | B. | NaCl和HCl | C. | I2和金刚石 | D. | NH3和H2O |
5.当萘与H2以物质的量比为1:1发生加成反应时,与1,3-丁二烯发生1,4-加成相似的产物有( )
①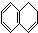 ②
② ③
③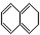 ④
④
①
 ②
② ③
③ ④
④
| A. | ①③ | B. | ②④ | C. | ②③ | D. | ①④ |
15.下列说法正确的是( )
①S8分子中 S原子采用的轨道杂化方式sp3
②C2H4分子中只有以s轨道与sp2杂化轨道“头碰头”方式重叠而成的σ键
③SnBr2分子中Sn-Br的键角<120°
④H3O+中H-O-H键角比H2O中H-O-H键角大.
①S8分子中 S原子采用的轨道杂化方式sp3
②C2H4分子中只有以s轨道与sp2杂化轨道“头碰头”方式重叠而成的σ键
③SnBr2分子中Sn-Br的键角<120°
④H3O+中H-O-H键角比H2O中H-O-H键角大.
| A. | ①② | B. | ③④ | C. | ①②③ | D. | ①③④ |
2.下列说法中错误的是( )
| A. | 需要加热才能发生的反应一定是吸热反应 | |
| B. | 化学键的断裂和形成是化学反应中能量变化的主要原因 | |
| C. | 化学反应中的能量变化通常表现为热量的变化 | |
| D. | 反应物总能量和生成物总能量的相对大小决定了反应是放出能量还是吸收能量 |
19.关于如图所示装置的叙述,错误的是( )


| A. | 锌是负极,其质量逐渐减轻 | |
| B. | 氢离子在铜的表面被还原,产生气泡 | |
| C. | 检流计的指针向右偏转 | |
| D. | 电流从锌片经导线流向铜片 |
14.下列离子反应方程式,书写正确的是( )
| A. | 向碳酸钠溶液中加过量盐酸 CO32-+2H+=H2O+CO2↑ | |
| B. | 向稀硫酸溶液中投入铁粉 2Fe+6H+=2Fe3++3H2↑ | |
| C. | 向盐酸中投入碳酸钙 CO32-+2H+=H2O+CO2↑ | |
| D. | .氢氧化钡溶液中加入硫酸 H++OH-=H2O |