题目内容
4.下列各表述与示意图一致的是(| A. | 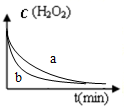 图表示双氧水分解时反应物浓度随时间的变化情况,a为加入少量FeCl3时的变化情况 | |
| B. | 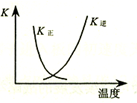 图中曲线表示反应2SO2(g)+O2(g)═2SO3(g);△H<0 正、逆反应的平衡常数K随温度的变化 | |
| C. | 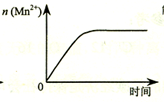 图表示10 mL 0.01 mol•L-1 KMnO4 酸性溶液与过量的0.1 mol•L-1 H2C2O4溶液混合时,n(Mn2+) 随时间的变化 | |
| D. | 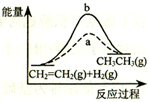 图中a、b曲线分别表示反应CH2=CH2 (g)+H2(g)→CH3CH3(g);△H>0反应过程中的能量变化,a为不加催化剂时的过程 |
分析 A、b反应速率快,表示加入了少量FeCl3;
B、则升高温度,平衡逆向移动,升温K逆应该增大,而K正应该减小,且正逆反应的平衡常数互为倒数关系;
C、该反应是放热反应,反应生成的Mn2+对该反应有催化作用,故反应速率越来越快,不是恒定速率;
D、因该反应是放热反应,但图象描述是吸热反应.
解答 解:A、双氧水分解时反应物浓度随时间的变化情况,b反应速率快,表示加入了少量FeCl3,故A错误;
B、因反应为放热反应,则升高温度,平衡逆向移动,升温K逆应该增大,而K正应该减小,且正逆反应的平衡常数互为倒数关系,故B正确;
C、该反应是放热反应,反应生成的Mn2+对该反应有催化作用,故反应速率越来越快,不是恒定速率,故C错误;
D、因该反应是放热反应,应反应物的总能量大于生成物的总能量,但图象描述是吸热反应,故D错误.
故选B.
点评 本题结合图象考查了中和滴定、化学平衡移动、氧化还原反应、反应中的能量变化,这些知识点是新课程改革考查的重点,明确考点“形变神不变”,做到善于抓规律.

练习册系列答案
相关题目
9.由于做实验时不小心使皮肤粘上了一些高锰酸钾粉末,形成的黑斑很久才能消除.如果用草酸(乙二酸)的稀溶液洗涤,黑斑可以迅速褪去,其离子方程式为:MnO4-+C2O42-+H+→CO2↑+Mn2++□. 则下列有关叙述正确的是.
| A. | 发生还原反应的是C2O42- | |
| B. | 该离子方程式右侧方框内的产物是OH- | |
| C. | 10mol H+参加反应时,电子转移5mol | |
| D. | 1mol草酸分子中含有9mol共用电子对 |
7.下列物质中,既能发生消去反应,又能催化氧化生成醛的是( )
| A. | CH3OH | B. | C2H5OH | C. | (CH3)3COH | D. | (CH3)3CCH2OH |
14.下列理解中正确的是( )
| A. | 有机物一定含有C元素 | |
| B. | 能够写出电离方程式的物质在书写离子方程式中一定可以拆 | |
| C. | 有机物中不可能含有金属元素 | |
| D. | AlCl3 属于离子化合物 |
9.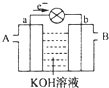 如图是一氧化碳空气燃料电池的工作原理示意图,a、b均为惰性电极.下列叙述中,正确的是( )
如图是一氧化碳空气燃料电池的工作原理示意图,a、b均为惰性电极.下列叙述中,正确的是( )
 如图是一氧化碳空气燃料电池的工作原理示意图,a、b均为惰性电极.下列叙述中,正确的是( )
如图是一氧化碳空气燃料电池的工作原理示意图,a、b均为惰性电极.下列叙述中,正确的是( )| A. | a电极发生还原反应,b电极发生氧化反应 | |
| B. | a电极的电极反应式为:CO+4OH-+2e-=CO2+2H2O | |
| C. | A处通入的是空气,B处通入的是CO | |
| D. | 用这种电池作电源精炼铜,若阴极质量增加6.4 g,则至少消耗标准状况下的CO 2.24 L |
13.X、Y、Z、T四种原子序数递增的短周期元素,其部分性质或结构如下:
下列说法正确的是( )
| 元素编号 | 元素性质或原子结构 |
| X | 形成的简单阳离子核外无电子 |
| Y | 元素的气态氢化物和它的最高价氧化物对应的水化物能发生化合反应 |
| Z | 元素在周期表的族序数等于周期序数的3倍 |
| T | 同周期元素中形成的简单离子半径最小 |
| A. | 原子半径大小顺序:T>Z>Y>X | |
| B. | 常温下,T的单质与Y的最高价氧化物对应水化物的浓溶液反应生成氢气 | |
| C. | X分别与Y、Z均可形成既含极性键又含非极性键的化合物 | |
| D. | 由X、Y和Z三种元素构成的强电解质,对水电离均起抑制作用 |
14.原子序数小于18的八种连号元素,它们单质的熔点随原子序数增大而变化的趋势如图所示.图中X元素应属( )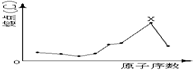

| A. | ⅢA族 | B. | ⅣA族 | C. | ⅤA族 | D. | ⅥA族 |
 短周期元素A、B、C、D在周期表中的位置如图,E2+与D的简单阴离子有相同的电子层结构,回答下列问题:
短周期元素A、B、C、D在周期表中的位置如图,E2+与D的简单阴离子有相同的电子层结构,回答下列问题: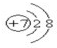 ,元素D位于元素周期表的第ⅥA族.
,元素D位于元素周期表的第ⅥA族.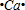 +2
+2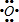 →
→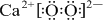 .
.