题目内容
下列有关元素的性质及其递变规律正确的是( )
| A、第二周期元素从左到右,最高正价从+1递增到+7 |
| B、ⅠA族与ⅦA族元素间既可形成共价化合物,也可形成离子化合物 |
| C、同主族元素从上到下,元素的非金属性逐渐增强 |
| D、同周期金属元素的化合价越高,其原子失电子能力越强 |
考点:同一主族内元素性质递变规律与原子结构的关系,非金属在元素周期表中的位置及其性质递变的规律,元素周期律的作用
专题:元素周期律与元素周期表专题
分析:A.第二周期中,O、F没有正价;
B.ⅠA族包含H和碱金属;
C.同主族元素从上到下,电子层增大,得电子能力减弱;
D.同周期金属元素的化合价越高,失电子能力越弱.
B.ⅠA族包含H和碱金属;
C.同主族元素从上到下,电子层增大,得电子能力减弱;
D.同周期金属元素的化合价越高,失电子能力越弱.
解答:
解:A.第二周期中,O、F没有正价,第二周期元素从左到右,最高正价从+1递增到+5,故A错误;
B.ⅠA族包含H和碱金属,H与ⅦA族元素间可形成共价化合物,碱金属与ⅦA族元素间形成离子化合物,故B正确;
C.同主族元素从上到下,电子层增大,得电子能力减弱,则元素的非金属性逐渐减弱,故C错误;
D.同周期金属元素的化合价越高,失电子能力越弱,则元素的金属性逐渐减弱,故D错误;
故选B.
B.ⅠA族包含H和碱金属,H与ⅦA族元素间可形成共价化合物,碱金属与ⅦA族元素间形成离子化合物,故B正确;
C.同主族元素从上到下,电子层增大,得电子能力减弱,则元素的非金属性逐渐减弱,故C错误;
D.同周期金属元素的化合价越高,失电子能力越弱,则元素的金属性逐渐减弱,故D错误;
故选B.
点评:本题考查元素的性质及比较,为高频考点,把握同周期、同主族元素性质的变化规律为解答的关键,侧重规律性知识的考查,选项A为易错点,题目难度不大.

练习册系列答案
相关题目
化学与生活息息相关,下列说法正确的是( )
| A、二氧化硫可广泛的用于食品的漂白 |
| B、正常雨水的pH为7,酸雨的pH小于5.6 |
| C、煤经过气化和液化等物理变化可以转化为清洁燃料 |
| D、“地沟油”禁止食用,但可以用来制肥皂等 |
下列离子方程式与所述事实相符且正确的是( )
| A、漂白粉溶液在空气中失效:ClO-+CO2+H2O═HClO+HCO3- |
| B、向Na2SO3溶液中通入足量氯气:SO32-+Cl2+H2O═SO42-+2Cl-+2H+ |
| C、用浓盐酸与MnO2反应制取少量氯气:MnO2+2H++2Cl-═Mn2++Cl2↑+2H2O |
| D、钠与CuSO4溶液反应:2Na+Cu2+═Cu+2Na+ |
物质的量浓度相同的NaCl、Na2SO4、Na3PO4三种溶液,当它们的体积比为1:2:3时,三种溶液中Na+的物质的量之比为( )
| A、1:1:1 |
| B、1:2:3 |
| C、3:2:1 |
| D、1:4:9 |
《关于宣传吸烟有毒与控制吸烟》的通知中规定:“中学生不准吸烟”.香烟燃烧产生的烟气中尼古丁(C10H14N2)对人体危害最大,下列说法正确的是( )
| A、尼古丁中氮元素的质量分数为17.3% |
| B、尼古丁中C、H、N三种元素的质量比为5:7:1 |
| C、尼古丁的摩尔质量是162 g |
| D、尼古丁是一种高分子化合物 |
推断乙酰水杨酸(如图)不具有的化学性质( )
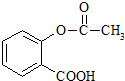

| A、与NaOH溶液反应 |
| B、水解反应 |
| C、与乙酸发生酯化反应 |
| D、与乙醇发生酯化反应 |
X、Y、Z、W、M均为短周期元素,X、Y同主族,X的氢化物和最高价氧化物的水化物能反应生成一种离子化合物,其水溶液显酸性;Z、W、M是第3周期连续的三种元素,其中只有一种是非金属,且原子半径Z>W>M.下列叙述准确的是( )
| A、X、M两元素氢化物的稳定性:X<M |
| B、Z、W、M的氧化物均可做耐高温材料 |
| C、Z是海水中含量最高的金属元素,W是地壳中含量最多的金属元素 |
| D、Z、W、M的单质均能与稀硫酸反应制取氢气,但反应剧烈程度依次减弱 |
下列元素中,非金属性最强的是( )
| A、P | B、S | C、Cl | D、Ar |
