题目内容
化学与生活息息相关,下列说法正确的是( )
| A、二氧化硫可广泛的用于食品的漂白 |
| B、正常雨水的pH为7,酸雨的pH小于5.6 |
| C、煤经过气化和液化等物理变化可以转化为清洁燃料 |
| D、“地沟油”禁止食用,但可以用来制肥皂等 |
考点:二氧化硫的化学性质,化石燃料与基本化工原料,油脂的性质、组成与结构
专题:元素及其化合物,有机化学基础
分析:A.二氧化硫有毒;
B.正常雨水的pH为5.6;
C.煤经过气化生成CO和氢气,液化生成甲醇;
D.“地沟油”的成分为油脂,对人体有害.
B.正常雨水的pH为5.6;
C.煤经过气化生成CO和氢气,液化生成甲醇;
D.“地沟油”的成分为油脂,对人体有害.
解答:
解:A.二氧化硫有毒,具有漂白性,但不能用于食品的漂白,故A错误;
B.正常雨水的pH为5.6,酸雨的pH小于5.6,故B错误;
C.煤的气化生成CO和氢气,液化生成甲醇,则煤经过气化和液化等化学变化可以转化为清洁燃料,故C错误;
D.“地沟油”的成分为油脂,对人体有害,油脂在碱性条件下水解为皂化反应,则禁止食用,但可以用来制肥皂等,故D正确;
故选D.
B.正常雨水的pH为5.6,酸雨的pH小于5.6,故B错误;
C.煤的气化生成CO和氢气,液化生成甲醇,则煤经过气化和液化等化学变化可以转化为清洁燃料,故C错误;
D.“地沟油”的成分为油脂,对人体有害,油脂在碱性条件下水解为皂化反应,则禁止食用,但可以用来制肥皂等,故D正确;
故选D.
点评:本题考查较综合,涉及漂白性、酸雨、煤的综合利用及油脂的性质等,注重化学与生活的联系,题目难度不大,选项C为易错点.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
几种短周期元素的原子半径及主要化合价如下表,相关说法正确的是( )
| 元素代号 | L | M | X | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 |
| 主要化合价 | +2 | +3 | +6、-2 | +2 | -2 |
| A、离子半径大小:r(M3+)>r(T2-) |
| B、其中R的金属性最强 |
| C、煤和石油中存在X元素 |
| D、L、X形成的简单离子核外电子数相等 |
在一定条件下,将0.1L CO、0.2L CO2、0.1L NO、0.2L NO2和0.2L NH3混合,然后通过分别盛有足量蒸馏水、饱和碳酸氢钠溶液和氢氧化钠溶液的三个洗气瓶(洗气瓶排列顺序不确定).假设气体通过每个洗气瓶都能充分反映,则尾气(已干燥)( )
| A、不可能是单一气体 |
| B、不可能含有一氧化碳 |
| C、可能存在原气体中的两种气体 |
| D、成分与洗气瓶的排列顺序无关 |
金属的冶炼常涉及氧化还原反应.由下列物质冶炼相应金属时采用电解法的是( )
| A、Al2O3 |
| B、HgO |
| C、Cu2S |
| D、Fe2O3 |
下列表述正确的是( )
①浓硝酸通常保存在棕色试剂瓶中
②检验亚硫酸钠溶液在空气中放置是否变质可以先加硝酸溶液,再加氯化钡溶液来检验
③锌与稀硝酸反应可以得到氢气
④浓硫酸滴到纸张上变黑,说明浓硫酸具有吸水性
⑤二氧化硫和二氧化氮都能形成酸雨,酸雨的pH等于5.6.
①浓硝酸通常保存在棕色试剂瓶中
②检验亚硫酸钠溶液在空气中放置是否变质可以先加硝酸溶液,再加氯化钡溶液来检验
③锌与稀硝酸反应可以得到氢气
④浓硫酸滴到纸张上变黑,说明浓硫酸具有吸水性
⑤二氧化硫和二氧化氮都能形成酸雨,酸雨的pH等于5.6.
| A、①③ | B、①② | C、① | D、①②④⑤ |
下列与有机物结构、性质相关的叙述错误的是( )
A、乙醛和丙烯醛(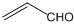 )不是同系物,但它们与H2充分反应后的产物是同系物 )不是同系物,但它们与H2充分反应后的产物是同系物 |
B、一分子β-月桂烯(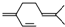 )与两分子溴发生加成反应的产物(只考虑位置异构)理论上最多有3种 )与两分子溴发生加成反应的产物(只考虑位置异构)理论上最多有3种 |
C、用甘氨酸(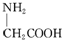 )和丙氨酸( )和丙氨酸(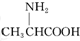 )缩合最多可形成4种二肽 )缩合最多可形成4种二肽 |
D、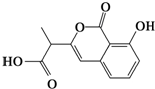 和 和 都既能与NaOH溶液反应,能与溴水反应,但与两种试剂反应的原因都不完全相同 都既能与NaOH溶液反应,能与溴水反应,但与两种试剂反应的原因都不完全相同 |
下列实验现象的描述错误的是( )
| A、氢气在氯气中燃烧产生苍白色火焰 |
| B、红热的铁丝在氯气中燃烧,火星四射,生成黑色固体颗粒 |
| C、红热的铜丝在氯气中燃烧,产生棕黄色烟 |
| D、钠在空气中燃烧,发出黄色的火焰,生成淡黄色固体 |
下列有关元素的性质及其递变规律正确的是( )
| A、第二周期元素从左到右,最高正价从+1递增到+7 |
| B、ⅠA族与ⅦA族元素间既可形成共价化合物,也可形成离子化合物 |
| C、同主族元素从上到下,元素的非金属性逐渐增强 |
| D、同周期金属元素的化合价越高,其原子失电子能力越强 |