题目内容
X、Y、Z、W、M均为短周期元素,X、Y同主族,X的氢化物和最高价氧化物的水化物能反应生成一种离子化合物,其水溶液显酸性;Z、W、M是第3周期连续的三种元素,其中只有一种是非金属,且原子半径Z>W>M.下列叙述准确的是( )
| A、X、M两元素氢化物的稳定性:X<M |
| B、Z、W、M的氧化物均可做耐高温材料 |
| C、Z是海水中含量最高的金属元素,W是地壳中含量最多的金属元素 |
| D、Z、W、M的单质均能与稀硫酸反应制取氢气,但反应剧烈程度依次减弱 |
考点:原子结构与元素周期律的关系
专题:元素周期律与元素周期表专题
分析:X、Y、Z、W、M均为短周期元素,X、Y同主族,X的氢化物和最高价氧化物的水化物能反应生成一种离子化合物,其水溶液显酸性,则X为N元素,Y为P元素;Z、W、M是第3周期连续的三种元素,其中只有一种是非金属,且原子半径Z>W>M,M是非金属元素,Z为Mg、W为Al、M为Si元素,再结合物质性质及元素周期律解答.
解答:
解:X、Y、Z、W、M均为短周期元素,X、Y同主族,X的氢化物和最高价氧化物的水化物能反应生成一种离子化合物,其水溶液显酸性,则X为N元素,Y为P元素;Z、W、M是第3周期连续的三种元素,其中只有一种是非金属,且原子半径Z>W>M,M是非金属元素,Z为Mg、W为Al、M为Si元素,
A.X、M两元素分别是N、Si元素,元素的非金属性越强其氢化物越稳定,非金属性N>Si,所以氢化物的稳定性:X>M,故A错误;
B.Z、W、M的氧化物分别是MgO、Al2O3、SiO2,这几种物质的熔点都很高,所以均可做耐高温材料,故B正确;
C.海水中含量最高的金属元素是Na元素,Al是地壳中含量最多的金属元素,故C错误;
D.Si和稀硫酸不反应,故D错误;
故选B.
A.X、M两元素分别是N、Si元素,元素的非金属性越强其氢化物越稳定,非金属性N>Si,所以氢化物的稳定性:X>M,故A错误;
B.Z、W、M的氧化物分别是MgO、Al2O3、SiO2,这几种物质的熔点都很高,所以均可做耐高温材料,故B正确;
C.海水中含量最高的金属元素是Na元素,Al是地壳中含量最多的金属元素,故C错误;
D.Si和稀硫酸不反应,故D错误;
故选B.
点评:本题考查了原子结构和元素周期律,根据物质的性质及元素在周期表中的位置确定元素,再结合元素周期律分析解答,注意:能从海水中提取镁,但海水中含量最大的金属元素不是镁,为易错点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列与有机物结构、性质相关的叙述错误的是( )
A、乙醛和丙烯醛(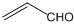 )不是同系物,但它们与H2充分反应后的产物是同系物 )不是同系物,但它们与H2充分反应后的产物是同系物 |
B、一分子β-月桂烯(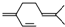 )与两分子溴发生加成反应的产物(只考虑位置异构)理论上最多有3种 )与两分子溴发生加成反应的产物(只考虑位置异构)理论上最多有3种 |
C、用甘氨酸(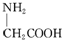 )和丙氨酸( )和丙氨酸(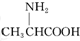 )缩合最多可形成4种二肽 )缩合最多可形成4种二肽 |
D、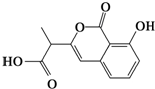 和 和 都既能与NaOH溶液反应,能与溴水反应,但与两种试剂反应的原因都不完全相同 都既能与NaOH溶液反应,能与溴水反应,但与两种试剂反应的原因都不完全相同 |
矿石中金的含量很低,金的性质又相当稳定,只能用湿法冶金--氰化法提炼,即采用稀的NaCN溶液处理已粉碎的矿石,把少量的金浸入溶液中,然后用金属锌作还原剂将金从溶液中置换析出.其反应原理为
①4Au+8NaCN+O2+2H2O═4Na[Au(CN)2]+4NaOH;
②2Na[Au(CN)2]+Zn═2Au+Na2[Zn(CN)4].
以下有关氰化法提炼金的说法中正确的是( )
①4Au+8NaCN+O2+2H2O═4Na[Au(CN)2]+4NaOH;
②2Na[Au(CN)2]+Zn═2Au+Na2[Zn(CN)4].
以下有关氰化法提炼金的说法中正确的是( )
| A、Na[Au(CN)2]不溶于水 |
| B、化合物Na[Au(CN)2]中金元素的化合价为+1 |
| C、金元素在地壳中能以化合态的形式存在 |
| D、在提炼过程中含金元素的物质始终作氧化剂 |
下列有关元素的性质及其递变规律正确的是( )
| A、第二周期元素从左到右,最高正价从+1递增到+7 |
| B、ⅠA族与ⅦA族元素间既可形成共价化合物,也可形成离子化合物 |
| C、同主族元素从上到下,元素的非金属性逐渐增强 |
| D、同周期金属元素的化合价越高,其原子失电子能力越强 |
下列化学变化中,能够一步实现的是( )
| A、Na→Na2O2 |
| B、Al2O3→Al(OH)3 |
| C、N2→HNO3 |
| D、S→SO3 |
为除去括号内的杂质,所选用的试剂或方法不正确的是( )
| A、NaHCO3溶液(Na2CO3溶液)通入过量的CO2 |
| B、铁粉(铝粉)加入适量的NaOH溶液过滤 |
| C、Na2CO3溶液(Na2SO4溶液)加入适量的Ba(OH)2溶液过滤 |
| D、CO2(CO)将混合气体通过足量灼热的CuO |
下列叙述正确的是( )
| A、乙烯、聚氯乙烯和苯分子中均含有碳碳双键 |
| B、淀粉、油脂、蛋白质都是天然高分子化合物且都能水解 |
| C、在蛋白质溶液中加入硫酸铜溶液,蛋白质会发生凝聚,加水后不能再溶解 |
| D、用氢氧化钠溶液,通过分液的方法,可以除去苯中的乙酸 |
下列叙述正确的是( )
| A、在氧化还原反应中,金属单质一般只作还原剂 |
| B、氧化还原反应中非金属单质一定是氧化剂 |
| C、金属元素被还原时所得产物一定是金属单质 |
| D、某元素从化合态变为游离态,该元素一定被还原 |