题目内容
推断乙酰水杨酸(如图)不具有的化学性质( )
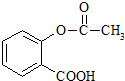

| A、与NaOH溶液反应 |
| B、水解反应 |
| C、与乙酸发生酯化反应 |
| D、与乙醇发生酯化反应 |
考点:有机物的结构和性质
专题:有机物的化学性质及推断
分析:由结构简式可知,分子中含-COOH、-COOC-,结合羧酸和酯的性质来解答.
解答:
解:A.-COOH、-COOC-均与NaOH反应,故A不选;
B.含-COOC-,可发生水解反应,故B不选;
C.不含-OH,则不能与乙酸发生酯化反应,故C选;
D.含-COOH,与乙醇发生酯化反应,故D不选;
故选C.
B.含-COOC-,可发生水解反应,故B不选;
C.不含-OH,则不能与乙酸发生酯化反应,故C选;
D.含-COOH,与乙醇发生酯化反应,故D不选;
故选C.
点评:本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重羧酸、酯性质的考查,题目难度不大.

练习册系列答案
 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案
相关题目
下列表述正确的是( )
①浓硝酸通常保存在棕色试剂瓶中
②检验亚硫酸钠溶液在空气中放置是否变质可以先加硝酸溶液,再加氯化钡溶液来检验
③锌与稀硝酸反应可以得到氢气
④浓硫酸滴到纸张上变黑,说明浓硫酸具有吸水性
⑤二氧化硫和二氧化氮都能形成酸雨,酸雨的pH等于5.6.
①浓硝酸通常保存在棕色试剂瓶中
②检验亚硫酸钠溶液在空气中放置是否变质可以先加硝酸溶液,再加氯化钡溶液来检验
③锌与稀硝酸反应可以得到氢气
④浓硫酸滴到纸张上变黑,说明浓硫酸具有吸水性
⑤二氧化硫和二氧化氮都能形成酸雨,酸雨的pH等于5.6.
| A、①③ | B、①② | C、① | D、①②④⑤ |
分子式为C4H7O2Br的有机物能与碳酸氢钠溶液反应产生气体,该有机物的结构可能有( )
| A、3种 | B、4种 | C、5种 | D、6种 |
MnO2和Zn是制造普通干电池的重要原料,工业上用软锰矿(主要成分MnO2)和闪锌矿(主要成分ZnS)来制取:
①将软锰矿、闪锌矿与硫酸共热:MnO2+ZnS+2H2SO4═MnSO4+ZnSO4+S+2H2O;
②除去反应混合物中的不溶物;
③电解混合物:MnSO4+ZnSO4+2H2O
MnO2+Zn+2H2SO4
下列说法错误的是( )
①将软锰矿、闪锌矿与硫酸共热:MnO2+ZnS+2H2SO4═MnSO4+ZnSO4+S+2H2O;
②除去反应混合物中的不溶物;
③电解混合物:MnSO4+ZnSO4+2H2O
| ||
下列说法错误的是( )
| A、干电池是一种将化学能转变为电能的装置 |
| B、步骤③电解时MnO2在阳极处生成,电极反应为:Mn2+-2e-+2H2O═MnO2+4H+ |
| C、步骤①每析出12.8g S沉淀,共转移0.8mol电子 |
| D、步骤③的反应也可以设计成原电池 |
下列有关元素的性质及其递变规律正确的是( )
| A、第二周期元素从左到右,最高正价从+1递增到+7 |
| B、ⅠA族与ⅦA族元素间既可形成共价化合物,也可形成离子化合物 |
| C、同主族元素从上到下,元素的非金属性逐渐增强 |
| D、同周期金属元素的化合价越高,其原子失电子能力越强 |
当光束通过下列分散系时,能观察到丁达尔效应的是( )
| A、硫酸铜溶液 | B、泥水 |
| C、葡萄糖注射液 | D、树林中的雾 |
为除去括号内的杂质,所选用的试剂或方法不正确的是( )
| A、NaHCO3溶液(Na2CO3溶液)通入过量的CO2 |
| B、铁粉(铝粉)加入适量的NaOH溶液过滤 |
| C、Na2CO3溶液(Na2SO4溶液)加入适量的Ba(OH)2溶液过滤 |
| D、CO2(CO)将混合气体通过足量灼热的CuO |
已知W、X、Y、Z为短周期元素,它们的原子半径依次增大,W与Z、X和Y分别同主族,Y、Z同周期.Z能与X形成两种常见的离子化合物,离子个数比均为2:1.下列说法错误的是( )
| A、Y、Z、X、W的原子序数依次减小 |
| B、W与X可形成既含极性共价键又含非极性共价键的化合物 |
| C、由W、X、Y、Z四种元素组成的常见化合物一定显酸性 |
| D、X的简单氢化物的沸点低于Y的简单氢化物的沸点 |
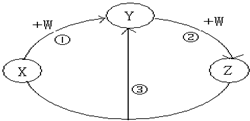 X、Y、Z、W都是中学化学常见的物质,其中X、Y、Z均含有同一种元素.在一定条件下相互转化的关系如图所示(部分反应中的H2O已略去).请按要求回答下列问题:
X、Y、Z、W都是中学化学常见的物质,其中X、Y、Z均含有同一种元素.在一定条件下相互转化的关系如图所示(部分反应中的H2O已略去).请按要求回答下列问题: