题目内容
下列离子方程式与所述事实相符且正确的是( )
| A、漂白粉溶液在空气中失效:ClO-+CO2+H2O═HClO+HCO3- |
| B、向Na2SO3溶液中通入足量氯气:SO32-+Cl2+H2O═SO42-+2Cl-+2H+ |
| C、用浓盐酸与MnO2反应制取少量氯气:MnO2+2H++2Cl-═Mn2++Cl2↑+2H2O |
| D、钠与CuSO4溶液反应:2Na+Cu2+═Cu+2Na+ |
考点:离子方程式的书写
专题:离子反应专题
分析:A.生成碳酸钙和次氯酸;
B.二者反应生成盐酸和硫酸钠;
C.二者反应需要加热且氢原子不守恒;
D.钠先和水反应生成NaOH和氢气,然后氢氧化钠再和硫酸铜发生复分解反应.
B.二者反应生成盐酸和硫酸钠;
C.二者反应需要加热且氢原子不守恒;
D.钠先和水反应生成NaOH和氢气,然后氢氧化钠再和硫酸铜发生复分解反应.
解答:
解:A.生成碳酸钙和次氯酸,离子方程式为Ca2++2ClO-+H2O+CO2=CaCO3+2HClO,故A错误;
B.二者反应生成盐酸和硫酸钠,离子方程式为SO32-+Cl2+H2O═SO42-+2Cl-+2H+,故B正确;
C.二者反应需要加热且氢原子不守恒,离子方程式为MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O,故C错误;
D.钠先和水反应生成NaOH和氢气,然后氢氧化钠再和硫酸铜发生复分解反应,离子方程式为2Na+2H2O+Cu2+=2Na++2OH-+H2↑+Cu(OH)2↓,故D错误;
故选B.
B.二者反应生成盐酸和硫酸钠,离子方程式为SO32-+Cl2+H2O═SO42-+2Cl-+2H+,故B正确;
C.二者反应需要加热且氢原子不守恒,离子方程式为MnO2+4H++2Cl-
| ||
D.钠先和水反应生成NaOH和氢气,然后氢氧化钠再和硫酸铜发生复分解反应,离子方程式为2Na+2H2O+Cu2+=2Na++2OH-+H2↑+Cu(OH)2↓,故D错误;
故选B.
点评:本题考查了离子方程式的书写,根据物质的性质、物质之间的反应及离子方程式书写规则判断,注意B中发生氧化还原反应、D中反应先后顺序,为易错点.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
几种短周期元素的原子半径及主要化合价如下表,相关说法正确的是( )
| 元素代号 | L | M | X | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 |
| 主要化合价 | +2 | +3 | +6、-2 | +2 | -2 |
| A、离子半径大小:r(M3+)>r(T2-) |
| B、其中R的金属性最强 |
| C、煤和石油中存在X元素 |
| D、L、X形成的简单离子核外电子数相等 |
下列与有机物结构、性质相关的叙述错误的是( )
A、乙醛和丙烯醛(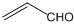 )不是同系物,但它们与H2充分反应后的产物是同系物 )不是同系物,但它们与H2充分反应后的产物是同系物 |
B、一分子β-月桂烯(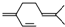 )与两分子溴发生加成反应的产物(只考虑位置异构)理论上最多有3种 )与两分子溴发生加成反应的产物(只考虑位置异构)理论上最多有3种 |
C、用甘氨酸(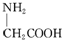 )和丙氨酸( )和丙氨酸(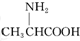 )缩合最多可形成4种二肽 )缩合最多可形成4种二肽 |
D、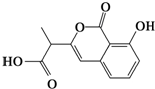 和 和 都既能与NaOH溶液反应,能与溴水反应,但与两种试剂反应的原因都不完全相同 都既能与NaOH溶液反应,能与溴水反应,但与两种试剂反应的原因都不完全相同 |
下列实验现象的描述错误的是( )
| A、氢气在氯气中燃烧产生苍白色火焰 |
| B、红热的铁丝在氯气中燃烧,火星四射,生成黑色固体颗粒 |
| C、红热的铜丝在氯气中燃烧,产生棕黄色烟 |
| D、钠在空气中燃烧,发出黄色的火焰,生成淡黄色固体 |
下列化合物中,既能发生消去反应生成烯烃,又能发生水解反应的是( )
| A、CH3CH2OH |
B、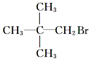 |
C、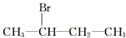 |
D、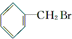 |
分子式为C4H7O2Br的有机物能与碳酸氢钠溶液反应产生气体,该有机物的结构可能有( )
| A、3种 | B、4种 | C、5种 | D、6种 |
矿石中金的含量很低,金的性质又相当稳定,只能用湿法冶金--氰化法提炼,即采用稀的NaCN溶液处理已粉碎的矿石,把少量的金浸入溶液中,然后用金属锌作还原剂将金从溶液中置换析出.其反应原理为
①4Au+8NaCN+O2+2H2O═4Na[Au(CN)2]+4NaOH;
②2Na[Au(CN)2]+Zn═2Au+Na2[Zn(CN)4].
以下有关氰化法提炼金的说法中正确的是( )
①4Au+8NaCN+O2+2H2O═4Na[Au(CN)2]+4NaOH;
②2Na[Au(CN)2]+Zn═2Au+Na2[Zn(CN)4].
以下有关氰化法提炼金的说法中正确的是( )
| A、Na[Au(CN)2]不溶于水 |
| B、化合物Na[Au(CN)2]中金元素的化合价为+1 |
| C、金元素在地壳中能以化合态的形式存在 |
| D、在提炼过程中含金元素的物质始终作氧化剂 |
下列有关元素的性质及其递变规律正确的是( )
| A、第二周期元素从左到右,最高正价从+1递增到+7 |
| B、ⅠA族与ⅦA族元素间既可形成共价化合物,也可形成离子化合物 |
| C、同主族元素从上到下,元素的非金属性逐渐增强 |
| D、同周期金属元素的化合价越高,其原子失电子能力越强 |
下列叙述正确的是( )
| A、在氧化还原反应中,金属单质一般只作还原剂 |
| B、氧化还原反应中非金属单质一定是氧化剂 |
| C、金属元素被还原时所得产物一定是金属单质 |
| D、某元素从化合态变为游离态,该元素一定被还原 |