题目内容
下列元素中,非金属性最强的是( )
| A、P | B、S | C、Cl | D、Ar |
考点:非金属在元素周期表中的位置及其性质递变的规律
专题:元素周期律与元素周期表专题
分析:根据同周期、同主族元素元素非金属性的递变规律来回答.
解答:
解:同周期元素从左到右,非金属性逐渐增强,所以非金属性:P<S<Cl,Ar为稀有气体,性质不活泼非金属性较弱,所以非金属性最强的是Cl.
故选C.
故选C.
点评:本题考查元素周期律知识,侧重于基础知识的考查,注意把握元素周期律的递变规律,难度不大.

练习册系列答案
相关题目
下列实验现象的描述错误的是( )
| A、氢气在氯气中燃烧产生苍白色火焰 |
| B、红热的铁丝在氯气中燃烧,火星四射,生成黑色固体颗粒 |
| C、红热的铜丝在氯气中燃烧,产生棕黄色烟 |
| D、钠在空气中燃烧,发出黄色的火焰,生成淡黄色固体 |
下列有关元素的性质及其递变规律正确的是( )
| A、第二周期元素从左到右,最高正价从+1递增到+7 |
| B、ⅠA族与ⅦA族元素间既可形成共价化合物,也可形成离子化合物 |
| C、同主族元素从上到下,元素的非金属性逐渐增强 |
| D、同周期金属元素的化合价越高,其原子失电子能力越强 |
为除去括号内的杂质,所选用的试剂或方法不正确的是( )
| A、NaHCO3溶液(Na2CO3溶液)通入过量的CO2 |
| B、铁粉(铝粉)加入适量的NaOH溶液过滤 |
| C、Na2CO3溶液(Na2SO4溶液)加入适量的Ba(OH)2溶液过滤 |
| D、CO2(CO)将混合气体通过足量灼热的CuO |
下列叙述正确的是( )
| A、乙烯、聚氯乙烯和苯分子中均含有碳碳双键 |
| B、淀粉、油脂、蛋白质都是天然高分子化合物且都能水解 |
| C、在蛋白质溶液中加入硫酸铜溶液,蛋白质会发生凝聚,加水后不能再溶解 |
| D、用氢氧化钠溶液,通过分液的方法,可以除去苯中的乙酸 |
已知W、X、Y、Z为短周期元素,它们的原子半径依次增大,W与Z、X和Y分别同主族,Y、Z同周期.Z能与X形成两种常见的离子化合物,离子个数比均为2:1.下列说法错误的是( )
| A、Y、Z、X、W的原子序数依次减小 |
| B、W与X可形成既含极性共价键又含非极性共价键的化合物 |
| C、由W、X、Y、Z四种元素组成的常见化合物一定显酸性 |
| D、X的简单氢化物的沸点低于Y的简单氢化物的沸点 |
下列叙述正确的是( )
| A、在氧化还原反应中,金属单质一般只作还原剂 |
| B、氧化还原反应中非金属单质一定是氧化剂 |
| C、金属元素被还原时所得产物一定是金属单质 |
| D、某元素从化合态变为游离态,该元素一定被还原 |
NA代表阿伏加德罗常数,下列说法正确的是( )
| A、9g D2O中含有的电子数为5NA |
| B、92g NO2和N2O4混合气体中含有原子数为6NA |
| C、1mol C3H8分子中共价键总数为8NA |
| D、65g Zn全部溶解在一定浓度的硝酸溶液中,有NO生成,则转移的电子数为NA |
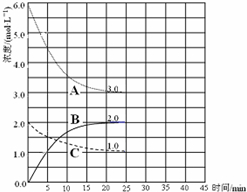 合成氨对农业生产及国防建设均具有重要意义.
合成氨对农业生产及国防建设均具有重要意义.