题目内容
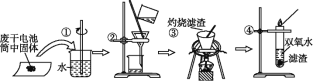
【题目】从含有CuCl2、FeCl2、FeCl3的工业废液中回收铜并制备氯化铁晶体的流程如下:
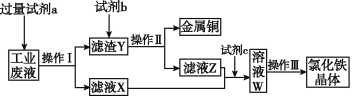
则下列说法正确的是
A. 试剂a是铁,试剂b是稀硫酸
B. 操作Ⅰ、操作Ⅱ、操作Ⅲ所用的仪器完全相同
C. 试剂c是氯气,反应的离子方程式为2Fe2++Cl2![]() 2Fe3++2Cl-
2Fe3++2Cl-
D. 用KSCN溶液可检验溶液W中是否有Fe2+
【答案】C
【解析】
从某含有FeCl2、FeCl3、CuCl2的工业废液中回收铜,工业废水中加入试剂a为过量的铁,操作Ⅰ为过滤,得到滤渣Y为Fe、Cu,滤液氯化亚铁溶液,滤渣Y中加入试剂b为盐酸溶解过量的铁生成氯化亚铁溶液,铜不溶,操作Ⅱ过滤得到铜和滤液Z为氯化亚铁溶液,滤液Z和X合并通入氯气,氧化亚铁离子为氯化铁溶液,蒸发结晶,过滤洗涤干燥得到氯化铁晶体,以此解答该题。
A.由最终得到FeCl3及其流程图可知,b为盐酸,若为硫酸会引入硫酸根杂质离子,故A错误;
B.上述分析可知,操作Ⅰ、Ⅱ是过滤,操作Ⅲ是蒸发结晶,过滤,所用仪器不同,故B错误;
C.滤液X,滤液Z中均含有FeCl2,c为氯气,氧化亚铁离子为铁离子反应为:2Fe2++Cl2═2Cl-+2Fe3+,故C正确;
D.KSCN溶液可检验溶液中是否含有Fe3+,检验Fe2+应选择铁氰化钾溶液,滴加后有蓝色沉淀,即说明溶液W中含有Fe2+,故D错误;
故答案为C。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目