题目内容
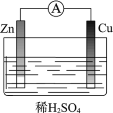
【题目】某原电池装置如图所示。其中,Zn电极为原电池的______极(填“正”或“负”),电极反应式是______________。Cu电极上发生的反应属于______(填“氧化”或“还原”) 反应。
【答案】负 Zn-2e=Zn2+ 还原
【解析】
在原电池反应中,活泼电极为负极,负极失去电子发生氧化反应;较不活泼电极为正极,正极上溶液中离子得到电子发生还原反应,据此分析解答。
有活动性不同的两个电极连接,形成闭合回路,有电解质溶液,因此构成了原电池。由于金属活动性:Zn>Cu,所以Zn为原电池的负极,失去电子,发生氧化反应,电极反应式为:Zn-2e=Zn2+;Cu不活泼,为原电池的正极,在正极上溶液中的H+得到电子,发生还原反应,电极方程式为:2H++2e-=H2↑。

练习册系列答案
 百年学典课时学练测系列答案
百年学典课时学练测系列答案 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案
相关题目