题目内容
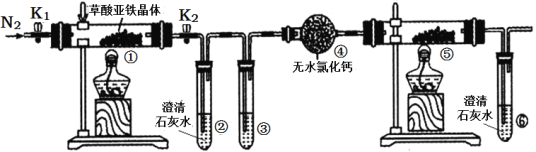
【题目】化学兴趣小组同学想用金属钠和空气制备纯度较高的Na2O2(N2不与金属钠应),可利用的装置如下。回答下列问题:
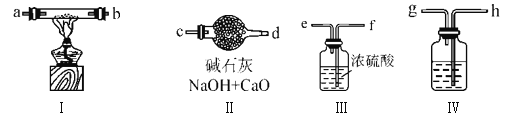
(1)装置Ⅳ中盛放的药品是________,若没有该装置可能导致生成的Na2O2中含有碳酸钠,其反应方程式为____________________________。
(2)若规定气体的气流方向从左到右,各仪器接口的标号字母(a、b……)顺序:
空气进入h,________接________,________接________,________接________,d
(3)装置Ⅱ的作用是_____________________________________________________。
(4)某学习小组发现:在盛有Na2O2的试管中加入足量水,固体完全溶解,并立即产生大量气泡,当气泡消失后,向其中滴入1~2滴酚酞溶液,溶液变红;将试管轻轻振荡,红色很快褪去;此时再向试管中加入少量MnO2粉末,又有气泡产生。
①使酚酞溶液变红是因为________________,红色褪去的可能原因是____________________。
② 加入MnO2反应的化学方程式为__________________________。
【答案】NaOH溶液 2Na2O2+2CO2===2Na2CO3+O2 g f e a b c 防止空气中的水蒸气和二氧化碳进入装置Ⅰ 过氧化钠和水反应生成氢氧化钠 反应生成的H2O2具有漂白作用 2H2O2![]() 2H2O+O2
2H2O+O2
【解析】
(1)装置Ⅳ是利用NaOH溶液除去空气中的二氧化碳,若没有该装置,空气的CO2和Na2O2反应会生成碳酸钠,发生反应方程式为2Na2O2 +2CO2 == 2Na2CO3 + O2↑;
(2)依据上述分析确定连接顺序,组合实验装置时各仪器的正确连接顺序为Ⅳ、Ⅲ、Ⅰ、Ⅱ,根据气流方向各接口的连接顺序为h g f e a b c;
(3)利用装置Ⅱ中有碱石灰防止空气中的水分和二氧化碳倒吸进入装置Ⅰ;
(4)①过氧化钠和水反应生成氢氧化钠是碱,碱遇酚酞变红;红色褪去的可能原因是过氧化钠和水反应生成的过氧化氢具有氧化性,能氧化有色物质,故答案为:过氧化钠和水反应生成碱氢氧化钠;反应生成的H2O2具有漂白作用;
②过氧化氢在二氧化锰做催化剂分解生成水和氧气,反应的化学方程式为:2H2O2![]() 2H2O+O2。
2H2O+O2。