题目内容
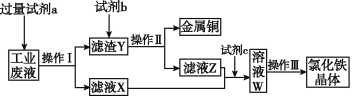
【题目】普通锌锰电池筒内无机物主要成分为MnO2、NH4Cl、ZnCl2等。某研究小组探究废于电池内的黑色固体并回收利用时,进行如图所示实验。下列有关实验的叙述正确的是
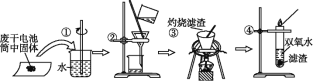
A. 操作①中玻璃棒的作用是转移固体 B. 操作②为过滤,得到的滤液显碱性
C. 操作③中盛放药品的仪器是坩埚 D. 操作④的目的是除去滤渣中的杂质
【答案】C
【解析】操作①中玻璃棒起到搅拌加速溶解的作用,A错误;普通锌锰电池筒内无机物质主要成分为MnO2、NH4Cl、ZnCl2等物质,NH4Cl、ZnCl2易溶于水,水解显酸性,MnO2难溶于水,操作②是把固体与溶液分离,应是过滤,得到的滤液显酸性,B错误;由图可知操作③是在坩埚内灼烧滤渣,通常把泥三角放在三角架上,再把坩埚放在泥三角上,C正确;二氧化锰是黑色固体,能作双氧水的催化剂,灼烧后的滤渣能加快双氧水分解产生氧气,能证明黑色固体是二氧化锰,所以该实验的目的不是除去滤渣中杂质,D错误;正确选项C。

 习题精选系列答案
习题精选系列答案【题目】根据电子排布三原理,填写下列空白。
(1)基态Mn2+的核外电子排布式为________。
(2)磷原子外围电子排布式为________。
(3)氧元素基态原子核外未成对电子数为________个。
【题目】下表为元素周期表的一部分,请参照元素①——⑨在表中的位置,回答问题
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA |
1 | ① | ||||||
2 | ② | ③ | ④ | ||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(1)表中⑧是用于半导体材料的元素,其元素符号为____,其在周期表中的位置是____。
(2)②、③、④的原子半径最小是____(填元素符号),其原子结构示意图是____。
(3)⑤、⑥、⑦的最高价氧化物对应的水化物,碱性最强的是____(填化学式)。
(4)①和③形成的原子个数比为1:1的化合物的电子式为____。
(5)⑤和⑨形成的化合物属于____(填“离子化合物”或“共价化合物”),用电子式表示其形成过程____