题目内容
10.0.1mol/L下列溶液:①H2SO4;②NH3•H2O; ③NaOH; ④NaCl;⑤NH4Cl;⑥CH3COONa;⑦HCl;⑧CH3COOH;⑨Ba(OH)2.pH值由大到小呈碱性的物质的顺序是⑨③②⑥,呈中性的物质是④,pH值由大到小的呈酸性物质的顺序是⑤⑧⑦①.
分析 一般来说,酸、强酸弱碱盐以及强酸的酸式盐溶液呈酸性,强酸强碱盐呈中性,碱、强碱若酸盐溶液呈碱性,以此解答该题.
解答 解:呈碱性的有:②NH3•H2O; ③NaOH;⑥CH3COONa;⑨Ba(OH)2,其中③⑨为强碱,⑨碱性最强,②为弱碱,⑥水解呈碱性,等浓度时pH最小,则pH值由大到小呈碱性的物质的顺序是⑨③②⑥,④NaCl为强酸强碱盐,溶液呈中性,呈酸性的有:①H2SO4;⑤NH4Cl;⑦HCl;⑧CH3COOH,其中①⑦为强酸,①酸性最强,⑧为弱酸,⑤水解呈酸性,等浓度时pH最大,则pH值由大到小的呈酸性物质的顺序是⑤⑧⑦①,
故答案为:⑨③②⑥;④;⑤⑧⑦①.
点评 本题综合考查pH的大小比较,为高频考点,侧重于学生的分析能力的考查,注意把握强弱电解质的比较以及盐类水解的原理,难度不大.

练习册系列答案
相关题目
20.下列物质所含分子数最多的是( )
| A. | 标准状况下22.4L CH4 | B. | 28g N2( N2的摩尔质量为28g/mol ) | ||
| C. | 1.5mol H2O | D. | 6.02×1023个NH3 |
1.下列物质的主要成分不是纤维的是( )
| A. | 纯棉布 | B. | 尼龙 | C. | 汽车轮胎 | D. | 晴纶 |
18.提高能源的利用率已成为国际能源研究的热点课题.下列相关措施使用不当的是( )
| A. | 使燃料充分燃烧 | B. | 加大能源开采力度 | ||
| C. | 加强能源利用的科技投入 | D. | 合理使用能源 |
5.下列解释实验事实的离子方程式不正确的是( )
| A. | 氧化铝与稀盐酸:Al2O3+6 H+═2 Al3++3H2O | |
| B. | 稀H2SO4与BaCl2溶液反应生成沉淀:Ba2++SO42-═BaSO4↓ | |
| C. | 用大理石与稀盐酸制备CO2:CaCO3+2H+═Ca2++CO2↑+H2O | |
| D. | 氯气与氯化亚铁溶液:Cl2+Fe2+═2Cl-+Fe3+ |
2.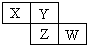 X、Y、Z、W均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子数是内层电子数的3倍,下列说法正确的是( )
X、Y、Z、W均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子数是内层电子数的3倍,下列说法正确的是( )
 X、Y、Z、W均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子数是内层电子数的3倍,下列说法正确的是( )
X、Y、Z、W均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子数是内层电子数的3倍,下列说法正确的是( )| A. | X的气态氢化物比Y的稳定 | |
| B. | W的最高价氧化物对应水化物的酸性比Z的强 | |
| C. | Z的非金属性比Y的强 | |
| D. | Y的氢化物只有一种 |