题目内容
15.(1)在水溶液中橙色的Cr2O72-与黄色的CrO42-有平衡关系:Cr2O72-+H2O?2CrO42-+2H+,把重铬酸钾溶于水配成稀溶液呈橙色.向上述溶液中加入几滴浓硫酸,溶液橙色变深(填“变深”“变浅”或“不变”),因为增大生成物浓度,平衡逆向移动,Cr2O72-浓度变大,颜色变深.
(2)已知2NO2(g)?N2O4(g)△H=-56.9kJ•mol-1,将NO2球浸泡在冰水中,气体的颜色变浅(填“变深”“变浅”或“不变”),原因是降温平衡正向移动,NO2浓度变小,颜色变浅.
(3)在烧杯里混合10mL 0.01mol/L FeC13溶液和10ml 0.01mol/L KSCN溶液,溶液立即变红.
已知反应:Fe3++3SCN-?Fe(SCN)3
①再向溶液中滴入1mol/LFeC13溶液,现象变深(变深、不变、变浅),平衡向正(正、逆)反应方向移动.
②在烧杯中加入KC1固体,颜色不变(变深、不变、变浅),平衡不移动.
分析 (1)加入酸,H+浓度增大,平衡左移,Cr2O72-浓度增大;
(2)正反应是放热反应,降低温度,平衡正向移动;
(3)①加入氯化铁,铁离子难度增大,平衡正向进行;硫氰酸钾难度减小;
②氯化钾对平衡无影响平衡不动.
解答 解:(1)加入酸,H+浓度增大,平衡左移,Cr2O72-浓度增大,溶液呈橙红色,故答案为:变深;因为增大生成物浓度,平衡逆向移动,Cr2O72-浓度变大,颜色变深;
(2)正反应是放热反应,降低温度,平衡正向移动,NO2浓度变小,气体的颜色变浅,故答案为:变浅;降温平衡正向移动,NO2浓度变小,颜色变浅;
(3)①FeCl3+3KSCN?Fe(SCN)3+3KCl反应,平衡为Fe3++3SCN-=Fe(SCN)3,滴入1mol/LFeC13溶液,铁离子浓度增大,平衡正向进行溶液颜色加深,平衡移动后KSCN浓度会减小,故答案为:变深;正;
②平衡为Fe3++3SCN-=Fe(SCN)3,加入KC1固体平衡不动,溶液颜色不变;故答案为:不变;不.
点评 本题考查化学平衡的影响因素,比较基础,注意建立平衡的微粒分析,题目较简单.

练习册系列答案
相关题目
5.下列应用或事实与胶体的性质没有关系的是( )
| A. | 在河流入海口处易形成三角州 | |
| B. | 用石膏或盐卤点制豆腐 | |
| C. | 尿毒症患者做“血液透析” | |
| D. | 在饱和氯化铁溶液中逐滴加入NaOH溶液,产生红褐色沉淀 |
6.关于氨基酸的叙述错误的是( )
| A. | 人体内氨基酸的分解代谢最终产物是水、二氧化碳和尿素 | |
| B. | 构成蛋白质的氨基酸分子的结构通式可以表示为: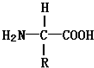 | |
| C. | 氨基酸只能和碱反应不能和酸反应 | |
| D. | 两个氨基酸通过脱水缩合形成二肽 |
3.人体内存在着酸碱平衡,如出现失衡将对人体健康产生极大危害.人体内生成的下列酸属于无机物的是( )
| A. | 乳酸(C3H6O3) | B. | 磷酸(H3PO4) | C. | 丙酮酸(C3H4O3) | D. | 乙酰乙酸(C4H6O3) |
20.有下列物质:①甲烷 ②丙烷 ③戊烷 ④2-甲基丁烷 ⑤2,2-二甲基丙烷,它们的沸点排列顺序正确的是( )
| A. | ①>②>③>④>⑤ | B. | ③>④>⑤>②>① | C. | ⑤>④>③>②>① | D. | ②>①>⑤>④>③ |
7.下列各组物质中,肯定全都属于纯净物的是( )
| A. | 液氯和氯水 | B. | 酒精溶液和乙醇 | ||
| C. | 七水合硫酸亚铁和硫酸亚铁 | D. | 干冰和混有冰的干冰 |
6.在相同条件下,下列各组中的物质按熔点由高到低排列的是( )
| A. | 干冰、冰、金属钠 | B. | 二氧化硅、食盐、硫 | ||
| C. | 金刚石、碘、氧化钙 | D. | HF、HCl、HBr |