题目内容
8.下列过程中,不可逆的是( )| A. | 蛋白质的盐析 | B. | 乙酸的电离 | ||
| C. | 酯在酸的催化下的水解 | D. | 蛋白质的变性 |
分析 A、蛋白质盐析是溶解度减小析出,加入水会继续溶解;
B、乙酸是弱电解质,存在电离平衡;
C、酯在酸催化剂作用下水解生成酸和醇,是可逆过程;
D、蛋白质变性是遇到重金属盐、加热、紫外线等使蛋白质失去生理活性.
解答 解:A、蛋白质盐析是溶解度减小析出,加入水会继续溶解,过程是可逆的,故A不符合;
B、乙酸是弱电解质,存在电离平衡部分电离,故B不符合;
C、酯在酸催化剂作用下水解生成酸和醇,水解过程是可逆过程,故C不符合;
D、蛋白质变性是遇到重金属盐、加热、紫外线等使蛋白质失去生理活性,是不可逆的过程,故D符合;
故选D.
点评 本题考查了可逆反应的特征分析应用,主要是理解物质性质的分析判断,掌握基础是关键,题目较简单.

练习册系列答案
相关题目
18.臭氧是理想的烟气脱硝剂,其脱硝反应为2NO2(g)+O3(g)?N2O5(g)+O2(g),在T温度下,向2.0L恒容密闭容器中充入2.0mol NO2和1.0mol O3,经过一段时间后达到平衡.反应过程中测定的部分数据见下表:
下列有关说法正确的是( )
| t/s | 0 | 3 | 6 | 12 | 24 |
| n(O2)/mol | 0 | 0.36 | 0.60 | 0.80 | 0.80 |
| A. | 反应在0~3 s内的平均速率v(NO2)=0.24 mol•L-1•s-1 | |
| B. | 24 s后,若保持其他条件不变,降低温度,达到新平衡时测得c(O2)=0.44 mol•L-1,则反应的△H<0 | |
| C. | 在T温度下,起始时向容器中充入1.0 mol NO2、0.5 mol O3和0.50 mol N2O5、0.50 mol O2,反应达到平衡时,压强为起始时的0.88倍 | |
| D. | 在T温度下,起始时向容器中充入2.0 mol N2O5和2.0 mol O2,达到平衡时,N2O5的转化率大于20% |
19.在一定条件下的恒温恒容容器中,当下列物理量不再发生变化时,表明反应:A(s)+3B(g)?2C(g)+D(g)已达平衡状态的是( )
| A. | 混合气体的压强 | |
| B. | 混合气体的密度 | |
| C. | 单位时间内生成0.5molA的同时,消耗1molC | |
| D. | V(C正):V(D正)=2:1 |
16.下列说法中正确的是( )
| A. | 主族元素的原子及其离子的核外电子层数等于该元素所在的周期数 | |
| B. | 元素周期表中从ⅢB到ⅡB族10个纵行的元素都是金属元素 | |
| C. | 稀有气体原子的最外层电子数都是8 | |
| D. | 互为同位素的元素物理性质、化学性质均相同 |
3.R、W、X、Y、Z为原子序数依次递增的同一短周期元素,下列说法一定正确的是(m、n均为正整数)( )
| A. | 若R(OH)n为强碱,则W(OH)n+1也为强碱 | |
| B. | 若最高氧化物的水化物HnXOm为强酸,则Y是活泼非金属元素 | |
| C. | 若Y的最低化合价为-2,则Z的最高正化合价为+6 | |
| D. | 若X的最高正化合价为+5,则五种元素都是非金属元素 |
20.下列电子是正确的是( )
| A. | 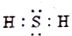 | B. | 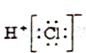 | C. | 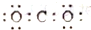 | D. | 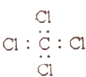 |
17.下列物质中,既含离子键、又含共价键的是( )
| A. | NaOH | B. | Na2O | C. | H2O | D. | CaCl2 |
18.下列物质一定属于同系物的是( )
①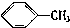 ②
②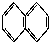 ③
③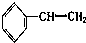 ④C2H4 ⑤CH2=CH-CH=CH2 ⑥C3H6 ⑦
④C2H4 ⑤CH2=CH-CH=CH2 ⑥C3H6 ⑦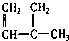 ⑧
⑧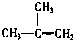
①
 ②
② ③
③ ④C2H4 ⑤CH2=CH-CH=CH2 ⑥C3H6 ⑦
④C2H4 ⑤CH2=CH-CH=CH2 ⑥C3H6 ⑦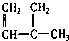 ⑧
⑧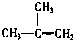
| A. | ①和 ② | B. | ④和⑥ | C. | ⑤和⑦; ④和⑧ | D. | ①和③ |