题目内容
18.等物质的量的乙烯与甲烷,所含分子数之比为1:1,碳原子个数之比为2:1,氢原子个数之比为1:1,若充分燃烧,消耗O2的体积比为3:2.0.1mol某烃在足量的氧气中完全燃烧,生成CO2和水各0.6mol,则该烃的分子式为C6H12.
分析 根据N=nNA可知,等物质的量的乙烯与甲烷,所含分子数相等,每个乙烯分子含有2个C原子、4个H原子,而每个甲烷分子含有1个C原子、4个H原子,可知碳原子数目之比为2:1,含有H原子数目相等.根据1molCxHy的耗氧量为(x+$\frac{y}{4}$)mol,计算二者耗氧量之比;
根据原子守恒计算烃的分子式.
解答 解:根据N=nNA可知,等物质的量的乙烯与甲烷,所含分子数之比为1:1,每个乙烯分子含有2个C原子、4个H原子,而每个甲烷分子含有1个C原子、4个H原子,可知碳原子数目之比为2:1,含有H原子数目之比为1:1.1mol乙烯耗氧量为(2+1)mol=3mol,1mol甲烷耗氧量为(1+1)mol=2mol,故等物质的量的乙烯与甲烷充分燃烧耗氧量之比为3mol:2mol=3:2;
0.1mol某烃在足量的氧气中完全燃烧,生成CO2和水各0.6mol,则该烃分子中N(C)=$\frac{0.6mol}{0.1mol}$=6、N(H)=$\frac{0.6mol×2}{0.1mol}$=12,故该烃的分子式为C6H12,
故答案为:1:1;2:1;1:1;3:2;C6H12.
点评 本题考查物质的量计算、化学方程式计算、有机物分子式确定,比较基础,侧重对基础知识的巩固.

练习册系列答案
 华东师大版一课一练系列答案
华东师大版一课一练系列答案 孟建平名校考卷系列答案
孟建平名校考卷系列答案
相关题目
10.室温下,甲、乙两烧杯均盛有5mL pH=3的某一元酸溶液,向乙烧杯中加水稀释至pH=4.关于甲、乙烧杯中溶液的描述正确的是( )
| A. | 溶液的体积10V甲≤V乙 | |
| B. | 水电离出的OH-浓度:10c(OH-)甲≤c(OH-)乙 | |
| C. | 若分别与5 mL pH=11的NaOH溶液反应,所得溶液的pH:甲≤乙 | |
| D. | 若分别用等浓度的NaOH溶液完全中和,所得溶液的pH:甲≤乙 |
8.下列如图装置应用于实验室制取NH3气体,并用AlCl3溶液吸收多余氨气制氢氧化铝,最后回收氯化铵的实验,能达到实验目的是( )
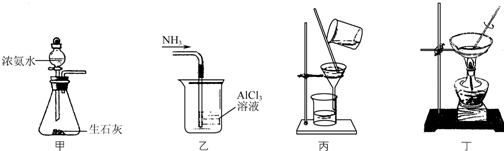

| A. | 用装置甲制取NH3 | |
| B. | 用装置乙吸收NH3制取Al(OH)3 | |
| C. | 用装置丙在不断搅拌下分离Al(OH)3和NH4Cl溶液 | |
| D. | 用装置丁蒸干NH4Cl溶液并灼烧制NH4Cl |
 H2CO3
H2CO3 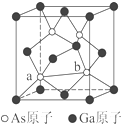 元素周期表第ⅤA族元素包括氮、磷、砷(As)、锑(Sb)等.这些元素无论在研制新型材料,还是在制作传统化肥、农药等方面都发挥了重要的作用.
元素周期表第ⅤA族元素包括氮、磷、砷(As)、锑(Sb)等.这些元素无论在研制新型材料,还是在制作传统化肥、农药等方面都发挥了重要的作用.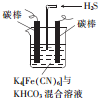 铁及其化合物在日常生活中应用广泛.
铁及其化合物在日常生活中应用广泛.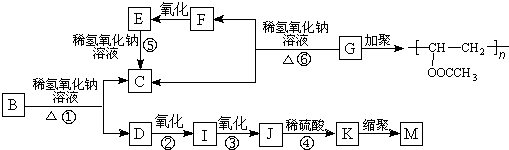
 .
. +3NaOH
+3NaOH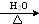 CH3COONa+
CH3COONa+ +NaBr+H2O.
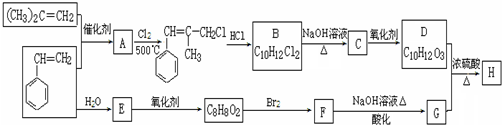
+NaBr+H2O. 、
、 .
.
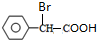 +2NaOH$\stackrel{△}{→}$
+2NaOH$\stackrel{△}{→}$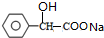 +NaBr+H2O.
+NaBr+H2O.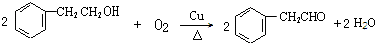 .
.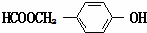 (写结构简式).
(写结构简式).