题目内容
【题目】元素![]() 、
、![]() 、
、![]() 、
、![]() 、
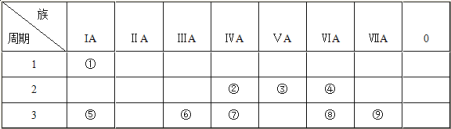
、![]() 在元素周期表2、3、4周期中,元素
在元素周期表2、3、4周期中,元素![]() 、
、![]() 、
、![]() 、
、![]() 与元素
与元素![]() 相邻,已知:
相邻,已知:![]() 元素为磷元素;
元素为磷元素;![]() 的氯化物分子呈正四面体结构:
的氯化物分子呈正四面体结构:![]() 与
与![]() 可以形成一种高温结构陶瓷;
可以形成一种高温结构陶瓷;![]() 的最高化合价氧化物的水化物是强酸。下列选项错误的是( )
的最高化合价氧化物的水化物是强酸。下列选项错误的是( )
A.![]() 的氧化物的晶体类型是共价晶体
的氧化物的晶体类型是共价晶体
B.![]() 的单质在空气中广泛存在
的单质在空气中广泛存在
C.![]() 和
和![]() 形成的化合物中,
形成的化合物中,![]() 可以呈现的最高化合价是
可以呈现的最高化合价是![]() 价
价
D.![]() 、
、![]() 、
、![]() 的氢化物中,沸点最低的是
的氢化物中,沸点最低的是![]() 的氢化物
的氢化物
【答案】D
【解析】
由“元素Q、R、W、Y、X在元素周期表2、3、4周期中,元素Q、R、W、Y与元素X相邻,且X元素为磷元素”可知Q、R、W、Y分别为N、Si、S、As中的一种。因为W的氯化物为正四面体型,则应为SiCl4,则W为Si,又W与Q形成高温陶瓷,高温陶瓷可联想到Si3N4 ,则Q为N,Y的最高价氧化的水化物为强酸,且与P相邻,则Y只能是S,R为As,所以Q、R、W、Y、X分别为N、As、Si、S、P。
A.![]() 的氧化物为SiO2,其晶体类型为原子晶体,又称共价晶体,A正确;
的氧化物为SiO2,其晶体类型为原子晶体,又称共价晶体,A正确;
B.![]() 的单质为N2,在空气中广泛存在,在空气中的体积分数约为78%,B正确;
的单质为N2,在空气中广泛存在,在空气中的体积分数约为78%,B正确;
C.R最外层电子数为5,则最高化合价为+5,在![]() 和
和![]() 形成的化合物中,R的最高价化合物应为As2S5,C正确;
形成的化合物中,R的最高价化合物应为As2S5,C正确;
D.![]() 、
、![]() 、
、![]() 的氢化物分别为NH3、AsH3、PH3,因三者中只有NH3分子间存在氢键,所以沸点最高,因相对分子质量AsH3>PH3,则AsH3分子间的作用力大于PH3,故沸点AsH3>PH3,氢化物沸点顺序为NH3>AsH3>PH3,所以沸点最低的是X的氢化物,D错误;
的氢化物分别为NH3、AsH3、PH3,因三者中只有NH3分子间存在氢键,所以沸点最高,因相对分子质量AsH3>PH3,则AsH3分子间的作用力大于PH3,故沸点AsH3>PH3,氢化物沸点顺序为NH3>AsH3>PH3,所以沸点最低的是X的氢化物,D错误;
答案选D。

练习册系列答案
相关题目