题目内容
【题目】![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 五种元素的原子序数依次递增。已知:①
五种元素的原子序数依次递增。已知:①![]() 位于周期表中第四周期
位于周期表中第四周期![]() 族,其余的均为短周期主族元素:②
族,其余的均为短周期主族元素:②![]() 的氧化物是光导纤维的主要成分;③
的氧化物是光导纤维的主要成分;③![]() 原子核外
原子核外![]() 层电子数为奇数;④
层电子数为奇数;④![]() 是形成化合物种类最多的元素;⑤
是形成化合物种类最多的元素;⑤![]() 原子
原子![]() 轨道的电子数为4。请回答下列问题:
轨道的电子数为4。请回答下列问题:
(1)写出一种![]() 元素形成氢化物的化学式_____________。
元素形成氢化物的化学式_____________。
(2)在1个由![]() 与
与![]() 形成的
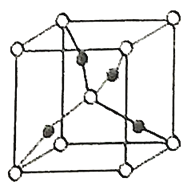
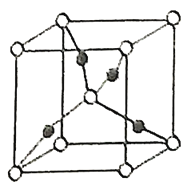
形成的![]() 晶胞中(结构如图所示)所包含的
晶胞中(结构如图所示)所包含的![]() 原子数目为____________个。
原子数目为____________个。
(3)在[F(NH3)4]2+离子中,![]() 的空轨道接受
的空轨道接受![]() 的氮原子提供的__________形成配位键。
的氮原子提供的__________形成配位键。
(4)常温下![]() 、
、![]() 和氢元素按原子数目1:1:2形成的气态常见物质
和氢元素按原子数目1:1:2形成的气态常见物质![]() 是__________(写名称),
是__________(写名称),![]() 物质分子中
物质分子中![]() 原子轨道的杂化类型为__________,
原子轨道的杂化类型为__________,![]() 分子中
分子中![]() 键的数目为__________
键的数目为__________![]() 。
。
(5)![]() 、
、![]() 、
、![]() 三种元素的第一电离能数值由小到大的顺序为__________(写元素符号)。
三种元素的第一电离能数值由小到大的顺序为__________(写元素符号)。
【答案】CH4 4 孤电子对 甲醛 sp2杂化 3 Si<C<N
【解析】
![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 五种元素的原子序数依次递增。根据①F位于周期表中第四周期
五种元素的原子序数依次递增。根据①F位于周期表中第四周期![]() 族可判断其为Cu;根据②E的氧化物是光导纤维的主要成分可判断E为Si;根据④X是形成化合物种类最多的元素可判断X为C;根据③Y原子核外L层电子数为奇数且原子序数比X的大可判断其属于第二周期的元素,可能为N或F;根据⑤Z的原子P轨道的电子数为4推测出Z可能为O或S,但E的原子序数大于Z,E为Si,所以Z只能为O,处于C和O之间的Y只能为N,所以
族可判断其为Cu;根据②E的氧化物是光导纤维的主要成分可判断E为Si;根据④X是形成化合物种类最多的元素可判断X为C;根据③Y原子核外L层电子数为奇数且原子序数比X的大可判断其属于第二周期的元素,可能为N或F;根据⑤Z的原子P轨道的电子数为4推测出Z可能为O或S,但E的原子序数大于Z,E为Si,所以Z只能为O,处于C和O之间的Y只能为N,所以![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 分别为C、N、O、Si、Cu,据此解题。
分别为C、N、O、Si、Cu,据此解题。
(1)X为C,![]() 元素形成的氢化物有很多,有烷烃、烯烃、炔烃等,其中的一种的化学式为CH4;
元素形成的氢化物有很多,有烷烃、烯烃、炔烃等,其中的一种的化学式为CH4;
(2)![]() 为Cu2O,根据化学式中原子个数比Cu:O=2:1,然后算出图中该晶胞的黑球个数为:1×4=4,白球个数为:8×1/8+1=2,所以黑球代表的是Cu原子,白球代表的是O原子,所以该晶胞中所包含的Cu原子数目为4个;
为Cu2O,根据化学式中原子个数比Cu:O=2:1,然后算出图中该晶胞的黑球个数为:1×4=4,白球个数为:8×1/8+1=2,所以黑球代表的是Cu原子,白球代表的是O原子,所以该晶胞中所包含的Cu原子数目为4个;
(3)在[Cu(NH3)4]2+离子中,![]() 的空轨道接受
的空轨道接受![]() 的氮原子提供的孤电子对形成配位键;
的氮原子提供的孤电子对形成配位键;
(4)常温下C、O和氢元素按原子数目1:1:2形成的气态常见物质![]() 是甲醛,甲醛分子中C原子可以形成四个化学键,因为碳的价电子数是4,其中,有两个单电子一起与氧的两个电子形成C=O,C剩余的两个单电子各与两个H形成两个C-H键,双键中含有一条σ键和一条π键,两条C-H单键都是σ键,所以σ键数=2+1=3,杂化轨道数=σ键数+孤对电子数(C无孤对电子,所以孤对电子数为0),所以杂化轨道数=3,为sp2杂化,1mol HCHO分子中σ键的数目为3
是甲醛,甲醛分子中C原子可以形成四个化学键,因为碳的价电子数是4,其中,有两个单电子一起与氧的两个电子形成C=O,C剩余的两个单电子各与两个H形成两个C-H键,双键中含有一条σ键和一条π键,两条C-H单键都是σ键,所以σ键数=2+1=3,杂化轨道数=σ键数+孤对电子数(C无孤对电子,所以孤对电子数为0),所以杂化轨道数=3,为sp2杂化,1mol HCHO分子中σ键的数目为3![]() ;
;
(5)![]() 、
、![]() 、
、![]() 三种元素分别为C、N、Si,根据每周期第一种元素电离能最小,最后一种元素的电离能最大,呈逐渐增大的趋势;同族元素从上到下第一电离能变小来进行判断,C、N、Si的第一电离能数值由小到大的顺序为:Si<C<N。
三种元素分别为C、N、Si,根据每周期第一种元素电离能最小,最后一种元素的电离能最大,呈逐渐增大的趋势;同族元素从上到下第一电离能变小来进行判断,C、N、Si的第一电离能数值由小到大的顺序为:Si<C<N。

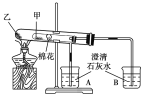
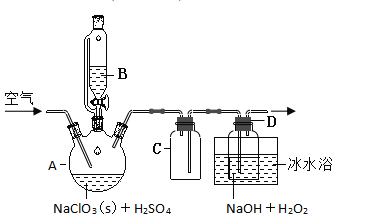
【题目】2019年4月23日,中国人民军成立70周年。提到海军就不得不提航空母舰,我国正在建造第三艘航空母舰。航母的龙骨要耐冲击,甲板要耐高温,外壳要耐腐蚀.
(1)镍铬钢抗腐蚀性能强,基态C r 原子价层电子的电子排布式为_______________。
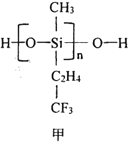
(2)航母甲板涂有一层耐高温的材料聚硅氧烷(结构如图申所示)。基态Si原子电子占据最高能级的电子云轮廓图为_______形:H、C、O、Si 四种元素中的电负性最高的是______。
(3)海洋是元素的摇篮,海水中含有大量卤族元素。
①钛卤化物的熔点如下表所示:
TiF4 | TiCl4 | TiBr4 | TiI4 | |
熔点/℃ | 377 | -24 | 38 | 150 |
解释表中卤化物之间熔点差异的原因是________________________。
②OF2的空间构型为___________,其中O原子杂化方式为__________杂化。
③氯元素可以形成多种含氧酸,其酸性由弱到强的顺序为:HClO <HClO2<HClO3<HClO4。试解释其酸性强弱的原因是_______________ 。
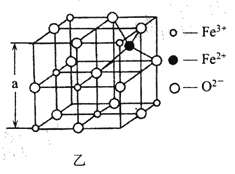
(4)海底金属软泥是在海洋底覆盖着的一层红棕色沉积物,蕴藏大着极的资源,含有硅、氧、锰、锌等。如图是从铁氧体离子晶体Fe3O4 中取出的能体现其晶体结构的一个立方体。
①晶体中的氧离子是否构成了面心立方最密堆积?________(填“是”或“否”);
②已知:Fe3O4 晶体的密度为5. 18gcm -3, 根据该图计算a________nrn (写出计算式即可,阿伏加德罗常数的值为N A)