题目内容
向恒温、恒容(2L)的密闭容器中充入2molX和一定量的Y,发生反应:2X(g)+Y(g)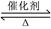 2Z(g)
2Z(g)
ΔH<0,4min后达到平衡c(X)=0.2mol·L-1,且X与Y的转化率相等。下列说法中不正确的是( )
| A.达到平衡时,再充入1molX,反应的焓变保持不变 |
| B.用Y表示4min内的反应速率为0.1 mol·L-1·min-1 |
| C.再向容器中充入1molZ,达到新平衡,c(X)∶c(Y)=2∶1 |
| D.4min后,若升高温度,平衡常数K增大 |
D
解析试题分析:A.达到平衡时,再充入1molX,由于反应的焓变与发生反应的物质的多少无关,因此焓变保持不变,正确;B.V(X)= 0.2mol/L÷4min=0.05mol/(L·min),V(X)=2V(Y),所以用Y表示4min内的反应速率为0.02 5mol/(L·min),错误;C.由于在反应容器内充入2molX和一定量的Y,达到平衡X与Y的转化率相等,说明Y是1mol,若再向容器中充入1molZ,则平衡逆向移动,由于产生的X、Y的物质的量的比是2:1,所以达到新平衡,c(X)∶c(Y)=2∶1,正确;D.4min后,若升高温度,根据平衡移动原理:升高温度,平衡向吸热反应方向移动,对该反应来说,平衡向逆反应方向移动,所以平衡常数K减小,错误。
考点:考查外界条件对化学反应速率、化学平衡的移动及平衡常数的影响的知识。

 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案 已知反应A2(g)+2B2(g) 2AB2(g)△H <0,下列说法正确的
2AB2(g)△H <0,下列说法正确的
| A.升高温度,正向反应速率增加,逆向反应速率减小 |
| B.升高温度有利于反应速率增加,从而缩短达到平衡的时间 |
| C.达到平衡后,升高温度或增大压强都有利于该反应平衡正向移动 |
| D.达到平衡后,降低温度或减小压强都有利于该反应平衡正向移动 |
在一定条件下,反应N2+3H2 2NH3,在2L密闭容器中进行,5min内氨的质量增加了1.7g,则反应速率为:
2NH3,在2L密闭容器中进行,5min内氨的质量增加了1.7g,则反应速率为:
| A.v(NH3)="0.1" mol/(L·min) | B.v(N2)="0.02" mol/(L·min) |
| C.v(H2)="0.015" mol/(L·min) | D.v(NH3)="0.17" mol/(L·min) |
已知:(NH4)2CO3(s)=NH4HCO3(s)+NH3(g) △H =" +" 74.9 kJ·mol-1,下列说法中正确的是
| A.该反应中熵变、焓变皆大于0 |
| B.该反应是吸热反应,因此一定不能自发进行 |
| C.碳酸盐分解反应中熵增加,因此任何条件下所有碳酸盐分解一定自发进行 |
| D.能自发进行的反应一定是放热反应,不能自发进行的反应一定是吸热反应 |
在一定温度下,10 mL 0.40mol/LH2O2溶液发生催化分解。不同时刻测得生成O2的体积(已折算为标准状况)如下表。下列叙述不正确的是(溶液体积变化忽略不计)
| t/min | 0 | 2 | 4 | 6 | 8 | 10 |
| V(O2)/mL | 0.0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 |
B.6~10 min的平均反应速率:v(H2O2)<3.3×10-2 mol/(L·min)
C.反应到6 min时,c(H2O2)=0.30mol/L
D.反应到6 min时,H2O2分解了50%
一定量的锌粉和6mol·L—1的过量盐酸反应,当向其中加入少量的下列物质:①石墨 ②CuO ③铜粉 ④锌粒 ⑤浓盐酸 ⑥无水乙酸 ⑦KNO3溶液 ⑧CuCl2时,能够加快反应速率,又不响产生H2总量的是 ( )
| A.①③④ | B.②④⑧ | C.①③⑤ | D.①⑤⑦ |
已知反应A2(g)+2B2 (g) 2AB2 (g)的ΔH<0,下列说法正确的是( )
2AB2 (g)的ΔH<0,下列说法正确的是( )
| A.升高温度,正向反应速率增加,逆向反应速率减小 |
| B.升高温度有利于反应速率增加,从而缩短达到平衡的时间 |
| C.达到平衡后,升高温度或增大压强都有利于该反应平衡正向移动 |
| D.达到平衡后,降低温度或减小压强都有利于该反应平衡正向移动 |
在一定温度下的定容密闭容器中,当下列条件不再改变时,表明反应: A(s)+2B(g) C(g)+D(g)已达到平衡状态的现象是
C(g)+D(g)已达到平衡状态的现象是
| A.混合气体的压强 | B.混合气体的密度 |
| C.气体的总物质的量 | D.单位时间内生成n mol C的同时消耗2n molB |
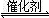 2CO2(g)+S(l) △H
2CO2(g)+S(l) △H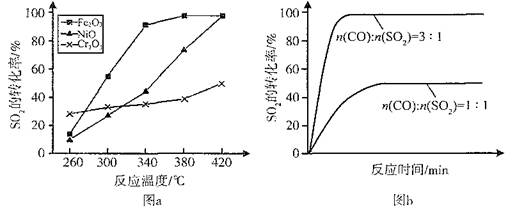
 HSO3—的平衡常数K="8.0" × 106 L?mol-1,计算时SO2、H2SO3的浓度忽略不计)
HSO3—的平衡常数K="8.0" × 106 L?mol-1,计算时SO2、H2SO3的浓度忽略不计)