��Ŀ����
����Ŀ������β���ѳ�Ϊ���п�������Ҫ��ȾԴ֮һ�����еĵ�����������Ҫ��Ⱦ�
��1��������ȼ������ʱ����NO��ԭ����ͼ1��ʾ��
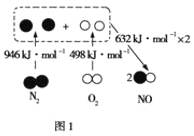
�÷�Ӧ���Ȼ�ѧ����ʽΪ______��
��2������β���ķ���֮һ�����������ϰ�װ��ת�������������·�Ӧ��2NO(g)��2CO(g)![]() N2(g)��2CO2(g) ��H��0������һ���¶��½�2mol NO��1mol CO����1L�̶��ݻ��������У���Ӧ�����и����ʵ�Ũ�ȱ仯��ͼ2��ʾ��
N2(g)��2CO2(g) ��H��0������һ���¶��½�2mol NO��1mol CO����1L�̶��ݻ��������У���Ӧ�����и����ʵ�Ũ�ȱ仯��ͼ2��ʾ��
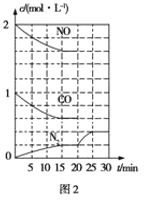
����ӿ�ʼ���ﵽƽ��״̬�Ĺ����У�ƽ����Ӧ������(CO2)=____�����¶��·�Ӧ��ƽ�ⳣ��K=____(���������λ��Ч����)
��20minʱ�ı������������____
A.����ѹǿ C.��СCO2Ũ���Ҹ��ø���Ч�Ĵ���
B.�����¶� D.�ں��º��������£�����He����
���������¶Ȳ��䣬20minʱ�������г���CO��N2��0.6mol��ƽ�⽫____(��������������������������)�ƶ���
��3���ý�̿��ԭNO2�ķ�ӦΪ��2NO2(g)��2C(s)![]() N2(g)��2CO2(g)���ں��������£���1L�ܱ������м��벻ͬ���ʵ�����NO2������C�����÷�Ӧ�����ƽ��ʱNO2��CO2�����ʵ���Ũ����ƽ����ѹǿ�Ĺ�ϵ��ͼ3��ʾ��
N2(g)��2CO2(g)���ں��������£���1L�ܱ������м��벻ͬ���ʵ�����NO2������C�����÷�Ӧ�����ƽ��ʱNO2��CO2�����ʵ���Ũ����ƽ����ѹǿ�Ĺ�ϵ��ͼ3��ʾ��
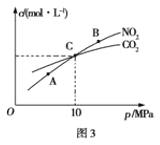
����������˵���÷�Ӧ�Ѵﵽƽ��״̬����_____
a.C���������� b. ���������ܶȲ��ٷ����ı�
c. v��(N2)������(CO2) d.����������ɫ���ٸı�
�ڼ���C��ʱ�÷�Ӧ��ƽ�ⳣ��Kp(C)=___(Kp����ƽ���ѹ����ƽ��Ũ�ȼ��㣬��ѹ=��ѹ�����ʵ�������)��
���𰸡�N2(g)��O2(g)=2NO(g) ��H=+180kJ��mol-1 0.027mol��L-1��min-1 0.035 C �� c 2
��������
(1)�����ʱ���H=��Ӧ��ļ���֮��-������ļ���֮�ͣ����ͼʾ�������
(2)�ٸ���ͼʾ�е�����Ũ�ȱ仯����ƽ��ʱ������̼��Ũ�ȣ�������ֵ�ƽ��Ũ�ȴ���ƽ�ⳣ������ʽK=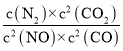 ���㣻��2NO(g)��2CO(g)
���㣻��2NO(g)��2CO(g)![]() N2(g)��2CO2(g)������ͼ��20minʱ������Ũ��������ƽ�����0.4 mol/L���ҽ���ƽ����Ҫ��ʱ����٣����Ӱ��ƽ���Ԫ�ط����жϣ��۸���Ũ����Qc��K�Ĵ�С�����жϣ�
N2(g)��2CO2(g)������ͼ��20minʱ������Ũ��������ƽ�����0.4 mol/L���ҽ���ƽ����Ҫ��ʱ����٣����Ӱ��ƽ���Ԫ�ط����жϣ��۸���Ũ����Qc��K�Ĵ�С�����жϣ�
(3)�ٸ���ƽ��״̬�������ͱ�־�����жϣ��ڸ�������ʽ���C��ʱNO2��CO2�����ʵ���Ũ����ȼ�����
(1)����ͼʾ��������ȼ������ʱ����NO��ԭ��ΪN2(g)��O2(g)=2NO(g)���ʱ���H=��Ӧ��ļ���֮��-������ļ���֮��=[946 kJ/mol +498 kJ/mol]-632 kJ/mol��2= +180kJ/mol���ʴ�Ϊ��N2(g)��O2(g)=2NO(g) ��H=+180kJ/mol��
(2)��ƽ��ʱ������Ũ��Ϊ0.2mol/L���������̼��ƽ��Ũ��Ϊ0.2mol/L��2=0.4mol/L��ƽ����Ӧ������(CO2)=![]() = 0.027mol��L-1��min-1���ɷ���ʽ2NO(g)��2CO(g)
= 0.027mol��L-1��min-1���ɷ���ʽ2NO(g)��2CO(g)![]() N2(g)��2CO2(g) ��H��0��֪��ƽ�ⳣ��K=
N2(g)��2CO2(g) ��H��0��֪��ƽ�ⳣ��K=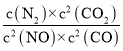 =
=![]() =
=![]() (L/mol)= 0.035���ʴ�Ϊ��0.027mol��L-1��min-1��0.035��
(L/mol)= 0.035���ʴ�Ϊ��0.027mol��L-1��min-1��0.035��
��2NO(g)��2CO(g)![]() N2(g)��2CO2(g)������ͼ��20minʱ������Ũ��������ƽ�����0.4 mol/L���ҽ���ƽ����Ҫ��ʱ����١�A.����ѹǿ����С�����������������Ũ�Ȼ�ͻȻ������ͼ������A����B. ����ӦΪ���ȷ�Ӧ�������¶ȣ�ƽ��������Ӧ�����ƶ���������Ũ����������Ӧ���ʼ���������ƽ����Ҫ��ʱ���������B����C.��СCO2Ũ�ȣ�ƽ�������ƶ���������Ũ���������������ƽ�ⲻһ�������ܹ����̽���ƽ����Ҫ��ʱ�䣬��C��ȷ��D.�ں��º��������£�����He���壬ƽ�ⲻһ����������Ũ�Ȳ��䣬��D���ʴ�Ϊ��C��
N2(g)��2CO2(g)������ͼ��20minʱ������Ũ��������ƽ�����0.4 mol/L���ҽ���ƽ����Ҫ��ʱ����١�A.����ѹǿ����С�����������������Ũ�Ȼ�ͻȻ������ͼ������A����B. ����ӦΪ���ȷ�Ӧ�������¶ȣ�ƽ��������Ӧ�����ƶ���������Ũ����������Ӧ���ʼ���������ƽ����Ҫ��ʱ���������B����C.��СCO2Ũ�ȣ�ƽ�������ƶ���������Ũ���������������ƽ�ⲻһ�������ܹ����̽���ƽ����Ҫ��ʱ�䣬��C��ȷ��D.�ں��º��������£�����He���壬ƽ�ⲻһ����������Ũ�Ȳ��䣬��D���ʴ�Ϊ��C��
���������¶Ȳ��䣬20minʱ���������г���CO��N2��0.6mol����Ũ����Qc=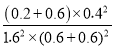 =
=![]() =K����ƽ�ⲻ�ƶ����ʴ�Ϊ������
=K����ƽ�ⲻ�ƶ����ʴ�Ϊ������
(3)��a.C���������䣬���������غ㶨�ɣ�˵���������ʵ�����Ҳ���䣬˵���ﵽ��ƽ��״̬����a��ѡ��b.���������ܶ������������������йأ����������ܶȲ��ٷ����ı䣬˵�����������������䣬˵���ﵽ��ƽ��״̬����b��ѡ��c.v��(N2)��2����(CO2)˵�����淴Ӧ������ȣ�v��(N2)������(CO2)��û�дﵽƽ��״̬����cѡ��d.����������ɫ���ٸı䣬˵������������Ũ�Ȳ��䣬˵���ﵽ��ƽ��״̬����d��ѡ���ʴ�Ϊ��c��
��1molNO2������C�����÷�Ӧ���跴Ӧ�Ķ������������ʵ���Ϊx��
2NO2(g)+2C(s)N2(g)+2CO2(g)
��ʼ(mol)�� 1 0 0
ת��(mol)�� x
ƽ��(mol)�� 1-x 0.5x x
��ͼ֪C��ʱNO2��CO2�����ʵ���Ũ����ȣ���1-x=x�����x=0.5����ƽ��ʱ�ܵ����ʵ���Ϊ1.25mol��C��ʱ�÷�Ӧ��ѹǿƽ�ⳣ��Kp(C)=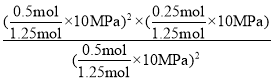 =2MPa���ʴ�Ϊ��2MPa(��2)��
=2MPa���ʴ�Ϊ��2MPa(��2)��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�