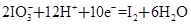题目内容
水热法制备Fe3O4纳米颗粒的反应是3Fe2++2S2O32-+O2+xOH—=Fe3O4+S4O62-+2H2O,下列说法中,正确的是
| A.Fe2+和S2O32—都是还原剂 |
| B.x=6 |
| C.1mol Fe2+被氧化时,被Fe2+还原的O2的物质的量为1/3mol |
| D.每生成1mol Fe3O4,反应转移的电子总数为3mol |
A
试题分析:A、根据方程式3Fe2++2S2O32-+O2+xOH—=Fe3O4+S4O62-+2H2O可知,铁元素和硫元素的化合价升高,因此Fe2+和S2O32—都是还原剂,A正确;B、根据氢原子守恒可知,反应的离子方程式为3Fe2++2S2O32-+O2+4OH-=Fe3O4+S4O62-+2H2O,即x=4,故B错误;C、1molFe2+被氧化时,失去1mol电子,则被Fe2+还原的O2的物质的量为
 mol,C不正确;D、反应3Fe2++2S2O32-+O2+4OH-=Fe3O4+S4O62-+2H2O中,Fe和S元素的化合价升高,被氧化,O2为氧化剂,每生成1molFe3O4,反应转移的电子总数为4mol,故D不正确,答案选A。
mol,C不正确;D、反应3Fe2++2S2O32-+O2+4OH-=Fe3O4+S4O62-+2H2O中,Fe和S元素的化合价升高,被氧化,O2为氧化剂,每生成1molFe3O4,反应转移的电子总数为4mol,故D不正确,答案选A。
练习册系列答案
相关题目
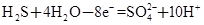 ②
②