��Ŀ����
ij��ѧѧϰС����̽�������仯����������Ժͻ�ԭ�ԡ�����Э���������ʵ�鱨�档
��1��ʵ��Ŀ�ģ�̽�������仯����������Ժͻ�ԭ��
��2��ʵ���Լ���������
�Լ����Ȼ�������Һ���Ȼ�����Һ����ˮ��KSCN��Һ�����ۡ�пƬ��ͭƬ��ϡ����
��������ͷ�ι��⣬����Ϊ��ʵ��ز����ٵ�һ�ֲ��������� ��
��3��ʵ���¼���ڷ��բ�ʵ�����𣬻��߲��ֲ�����д��
��4��ѧϰС���ͬѧ���ӱ�ʵ���л�õ�֪ʶ�ƹ㵽���������ʵ�ѧϰ�����ж��������ʼ������������л�ԭ�Ե���
A��Cl2 B��Na C��Mg2+ D��H2O2
��5����ʵ����У��в���ͬѧ���Ȼ�������Һ�е���KSCN��Һ�ͳ�����Ѫ��ɫ������Ϊ��ʲôԭ�� ��
�㽫��ʵ��Ա�������Ȼ�������Һʱ������Ľ����� ��
��6���������Ȼ�����Һʱ������ʵ��Աʧ���ܵ�����Һ�к���������Fe2����Ϊ����ʵ��Ա���м�������Fe2���Ĵ��ڣ��������������ѡ����ʵ��Լ��� ��
A��KSCN��Һ B��ϡ���� C��KMnO4��Һ D��NaOH��Һ
��1��ʵ��Ŀ�ģ�̽�������仯����������Ժͻ�ԭ��
��2��ʵ���Լ���������
�Լ����Ȼ�������Һ���Ȼ�����Һ����ˮ��KSCN��Һ�����ۡ�пƬ��ͭƬ��ϡ����
��������ͷ�ι��⣬����Ϊ��ʵ��ز����ٵ�һ�ֲ��������� ��
| ��� | ʵ����� | ʵ��۲죨��Ҫ���� | ���ӷ���ʽ | ��������� |
| �� | �������е� ��ϡ���� | �����ܽ⣬��Һ���� ɫ���dz��ɫ������ ɫ��ζ�ĵ��������� | Fe +2H��= H2��+ Fe2�� | Fe���л�ԭ�� |
| �� | �Ȼ�������Һ�е���KSCN��Һ���ټ�����ˮ | ����KSCN��Һ���� �Ա仯��������ˮ�� �����Ѫ��ɫ | | |
| �� | �Ȼ�������Һ�� ��пƬ | | Fe2��+ Zn =" Fe" + Zn 2+�� | |
| �� | | | | Fe3������������ |
��3��ʵ���¼���ڷ��բ�ʵ�����𣬻��߲��ֲ�����д��
��4��ѧϰС���ͬѧ���ӱ�ʵ���л�õ�֪ʶ�ƹ㵽���������ʵ�ѧϰ�����ж��������ʼ������������л�ԭ�Ե���
A��Cl2 B��Na C��Mg2+ D��H2O2
��5����ʵ����У��в���ͬѧ���Ȼ�������Һ�е���KSCN��Һ�ͳ�����Ѫ��ɫ������Ϊ��ʲôԭ�� ��
�㽫��ʵ��Ա�������Ȼ�������Һʱ������Ľ����� ��
��6���������Ȼ�����Һʱ������ʵ��Աʧ���ܵ�����Һ�к���������Fe2����Ϊ����ʵ��Ա���м�������Fe2���Ĵ��ڣ��������������ѡ����ʵ��Լ��� ��
A��KSCN��Һ B��ϡ���� C��KMnO4��Һ D��NaOH��Һ
��2���Թ� (1��)
��3����2Fe2+ +Cl2=2Fe3+ +2 Cl-(1��)��Fe3++3SCN- = Fe(KSCN)3��1�֣���Fe2+���л�ԭ��(1��)
�� Fe2+����������(1��)
�����Ȼ�����Һ�м���KSCN��Һ���ټ�������CuƬ�������ۻ�пƬ����(1��)
����KSCN��Һ����Ѫ��ɫ����������CuƬ�������ۻ�пƬ����Ѫ��ɫ��ʧ(1��)��
�����ȼ�������CuƬ�������ۻ�пƬ�����ټ���KSCN��Һ����Ѫ��ɫ���֣���
2Fe3+ +Cu = 2Fe2+ + Cu2�� ��2Fe3+ +Fe = 3Fe2+��2Fe3+ + Zn = 2Fe2+ + Zn 2����
2Fe3+ + 3Zn = 2Fe+3 Zn 2��(1��)
��4��AD (2��)
��5���Ȼ�������Һ�е�Fe2+������(2��)�������Ȼ�������ҺʱҪ��������������(2��)��
��6��C(2��)
��3����2Fe2+ +Cl2=2Fe3+ +2 Cl-(1��)��Fe3++3SCN- = Fe(KSCN)3��1�֣���Fe2+���л�ԭ��(1��)
�� Fe2+����������(1��)
�����Ȼ�����Һ�м���KSCN��Һ���ټ�������CuƬ�������ۻ�пƬ����(1��)
����KSCN��Һ����Ѫ��ɫ����������CuƬ�������ۻ�пƬ����Ѫ��ɫ��ʧ(1��)��
�����ȼ�������CuƬ�������ۻ�пƬ�����ټ���KSCN��Һ����Ѫ��ɫ���֣���
2Fe3+ +Cu = 2Fe2+ + Cu2�� ��2Fe3+ +Fe = 3Fe2+��2Fe3+ + Zn = 2Fe2+ + Zn 2����
2Fe3+ + 3Zn = 2Fe+3 Zn 2��(1��)
��4��AD (2��)
��5���Ȼ�������Һ�е�Fe2+������(2��)�������Ȼ�������ҺʱҪ��������������(2��)��
��6��C(2��)
�����������2����ȱ��Ӧ�������Թܡ�
��3���ڼ�����ˮ��Cl2��Fe2+����ΪFe3+�����ӷ���ʽΪ��2Fe2+ +Cl2=2Fe3+ +2 Cl-��Fe3+��SCN?������Ϸ�Ӧ��Fe3++3SCN- = Fe(KSCN)3��˵��Fe2+���л�ԭ�ԡ�
��Fe2��+ Zn =" Fe" + Zn 2+��Ӧ�У�FeԪ�صĻ��ϼ۽��ͣ�˵��Fe2+���������ԡ�
��Ҫ֤��Fe3�����������ԣ��ȼ���KSCN��Һ����Һ��죬�ټ��뻹ԭ������CuƬ�������ۻ�пƬ������ɫ��ʧ��˵��Fe3+���������ԣ�����ѡ����Լ�д�����ӷ���ʽ��
��4��Ԫ�ػ��ϼ۴����м��̬�����ʣ�����������Ҳ�л�ԭ�ԣ�Cl2��H2O2��ClԪ�غ�OԪ�ش����м��̬�����������ʼ���������Ҳ�л�ԭ�ԣ���A�D����ȷ��
��5�����Ȼ�������Һ�е���KSCN��Һ�ͳ�����Ѫ��ɫ������ΪFe2+���л�ԭ�ԣ�������ΪFe3+�������Ȼ�������Һʱ�������������ۣ��ɷ�ֹFe2+��������
��6��Fe2+���л�ԭ�ԣ���ʹKMnO4��Һ��ɫ����C����ȷ��

��ϰ��ϵ�д�
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
�����Ŀ
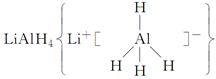 ��LiH���ǽ���������������л��ϳ��еij����Լ�����ˮ���ܾ��ҷ�Ӧ�ų�H2��LiAlH4��125 ��ֽ�ΪLiH��H2��Al������˵���в���ȷ���� (����)��
��LiH���ǽ���������������л��ϳ��еij����Լ�����ˮ���ܾ��ҷ�Ӧ�ų�H2��LiAlH4��125 ��ֽ�ΪLiH��H2��Al������˵���в���ȷ���� (����)�� ��������
�������� �ں���3molNaHSO3����Һ����μ���KIO3��Һ������KIO3������I2�����ʵ����Ĺ�ϵ��ͼ��ʾ��������˵���������( )
�ں���3molNaHSO3����Һ����μ���KIO3��Һ������KIO3������I2�����ʵ����Ĺ�ϵ��ͼ��ʾ��������˵���������( )
 N2O��+2H2O
N2O��+2H2O