��Ŀ����
���������һ�ֵ��͵�ǿ��������
���������գ�
������KMnO4������Һ����Cu2S��CuS�Ļ����ʱ�������ķ�Ӧ���£�
�� MnO4��+ Cu2S + H+�� Cu2+ + SO2�� + Mn2+ + H2O(δ��ƽ)
�� MnO4��+ CuS + H+ �� Cu2+ + SO2�� + Mn2+�� H2O(δ��ƽ)
��1�����й��ڷ�Ӧ�ٵ�˵���д������ ��ѡ���ţ���
a����������Ԫ����Cu��S
b���������뻹ԭ�������ʵ���֮��Ϊ8:5
c������2.24 L(�����) SO2��ת�Ƶ��ӵ����ʵ�����0.8 mol
d����ԭ�Ե�ǿ����ϵ�ǣ� Mn2+> Cu2S
��2�������Ӧ���е���ת�Ƶķ������Ŀ�� MnO4��+ CuS
����ϡ�����У�MnO4����H2O2Ҳ�ܷ���������ԭ��Ӧ
������Ӧ��H2O2��2e �� 2H+ + O2��
��ԭ��Ӧ��MnO4�� + 5e + 8H+ �� Mn2+ + 4H2O
��3����Ӧ������0.5 mol H2O2�μӴ˷�Ӧ��ת�Ƶ��ӵĸ���Ϊ ����������Ӧ�ó�������������ǿ���Ľ����� >___________(��д��ѧʽ)��
��4����֪��2KMnO4+ 7H2O2+3H2SO4�� K2SO4+2MnSO4 +6O2��+10H2O����1mol KMnO4������H2O2��
mol��
���������գ�
������KMnO4������Һ����Cu2S��CuS�Ļ����ʱ�������ķ�Ӧ���£�
�� MnO4��+ Cu2S + H+�� Cu2+ + SO2�� + Mn2+ + H2O(δ��ƽ)
�� MnO4��+ CuS + H+ �� Cu2+ + SO2�� + Mn2+�� H2O(δ��ƽ)
��1�����й��ڷ�Ӧ�ٵ�˵���д������ ��ѡ���ţ���
a����������Ԫ����Cu��S
b���������뻹ԭ�������ʵ���֮��Ϊ8:5
c������2.24 L(�����) SO2��ת�Ƶ��ӵ����ʵ�����0.8 mol
d����ԭ�Ե�ǿ����ϵ�ǣ� Mn2+> Cu2S
��2�������Ӧ���е���ת�Ƶķ������Ŀ�� MnO4��+ CuS
����ϡ�����У�MnO4����H2O2Ҳ�ܷ���������ԭ��Ӧ
������Ӧ��H2O2��2e �� 2H+ + O2��
��ԭ��Ӧ��MnO4�� + 5e + 8H+ �� Mn2+ + 4H2O
��3����Ӧ������0.5 mol H2O2�μӴ˷�Ӧ��ת�Ƶ��ӵĸ���Ϊ ����������Ӧ�ó�������������ǿ���Ľ����� >___________(��д��ѧʽ)��
��4����֪��2KMnO4+ 7H2O2+3H2SO4�� K2SO4+2MnSO4 +6O2��+10H2O����1mol KMnO4������H2O2��
mol��
��1��d ��2�֣�
��2�� 6MnO4��+ 5CuS ��2�֣�ϵ��1�֣�����ת�Ƶ���Ŀ�ͷ���1�֣�
��3��6.02��1023 ��1�֣��� KMnO4> H2O2(��O2) ��1�֣�
��4��2.5 ��2�֣�
��2�� 6MnO4��+ 5CuS ��2�֣�ϵ��1�֣�����ת�Ƶ���Ŀ�ͷ���1�֣�
��3��6.02��1023 ��1�֣��� KMnO4> H2O2(��O2) ��1�֣�
��4��2.5 ��2�֣�
�������������1��a����Ӧ��ͭԪ�ػ��ϼ۴�+1�����ߵ�+2�ۣ���Ԫ�ػ��ϼ۴�-2�����ߵ�+4�ۣ����ϼ����ߵ�Ԫ�ر����������Ա�������Ԫ����S��Cu����a��ȷ�� b����Ԫ�ػ��ϼ۽��ͣ���+7�۽���Ϊ+2�ۣ�Cu2SԪ�ػ��ϼ۶���������ԭ����1molMnO4-�õ�5mol���ӣ���Ӧ��ͭԪ�ػ��ϼ۴�+1�����ߵ�+2�ۣ���Ԫ�ػ��ϼ۴�-2�����ߵ�+4�ۣ�1molCu2Sʧȥ8mol���ӣ����������뻹ԭ�������ʵ���֮��Ϊ8��5����b��ȷ�� c������2.24LL������£�SO2ʱ�����ʵ���Ϊ0.1mol����Ӧ��Cu2S���ʵ���Ϊ0.1mol����Ӧ��ת�Ƶ��ӵ����ʵ����ǣ�
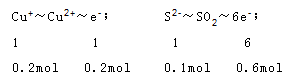
���Ե���ת�ƹ�0.8mol����c��ȷ�� d��������ԭ��Ӧ�л�ԭ���Ļ�ԭ�Դ��ڻ�ԭ����Ļ�ԭ�ԣ���ԭ�Ե�ǿ����ϵ�ǣ�Mn2+��Cu2S����d����ѡd��
��2����Ӧ����MnԪ�ػ��ϼ۽��ͣ���+7�۽���Ϊ+2�ۣ�1molMnO4-�õ�5mol���ӣ�CuS����Ԫ�ػ��ϼ۴�-2�����ߵ�+4�ۣ�1molCuSʧȥ6mol���ӣ���������ʵ���֮��Ϊ6��5��ת�Ƶ�����ĿΪ5��6=30���ɱ�ʾΪ
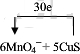 ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
����3����H2O2-2e��2H++O2����֪����Ӧ������0.5mol H2O2�μӴ˷�Ӧ��ת�Ƶ��ӵĸ���Ϊ0.5��2��NA=NA���ڷ�Ӧ��MnO4-Ϊ��������H2O2Ϊ��ԭ������������MnO4-��H2O2���ʴ�Ϊ��NA��MnO4-��H2O2��
��4����Ӧ2KMnO4+7H2O2+3H2SO4��K2SO4+2MnSO4+6O2��+10H2O�У�2molKMnO4������5molH2O2�����ɵ�6molO2�У���5molΪH2O2���������ɣ���1molΪH2O2��������������ԭ��Ӧ���ɣ���1mol KMnO4������H2O2��2.5mol���ʴ�Ϊ��2.5��

��ϰ��ϵ�д�
 ������ĩ��ϰ��ѵ��ϵ�д�
������ĩ��ϰ��ѵ��ϵ�д� С��ʿ��ĩ����100��ϵ�д�
С��ʿ��ĩ����100��ϵ�д�
�����Ŀ
