题目内容
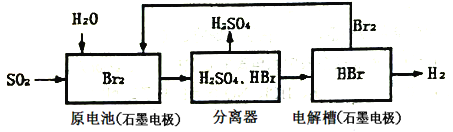
【题目】从海水中提取部分物质的过程如下图所示

下列有关说法错误的是
A. 过程①需要加入化学试剂、沉淀、过滤等操作
B. 由“母液→无水MgCl2”一系列变化中未涉及氧化还原反应
C. 工业上一般用金属钠与无水MgCl2反应制取Mg单质
D. 反应③和⑤均可由下列反应实现:2Br-+Cl2=Br2+2Cl-,该反应属于置换反应
【答案】C
【解析】
A.过程①在粗盐中含有CaCl2、MgCl2、Na2SO4等杂质,需要加入化学试剂Na2CO3、BaCl2、NaOH等化学试剂把杂质沉淀过滤除去,再加入HCl调节溶液的pH,就得到精盐溶液,可以用于氯碱工业,正确;
B.母液中含有MgCl2,将溶液在HCl的氛围中加热就可以得到无水MgCl2,在这一系列变化中元素的化合价没有变化,因此未涉及氧化还原反应,正确;
C.工业上一般电解无水MgCl2反应制取Mg单质,错误;
D.反应③和⑤均可由下列反应实现:2Br-+Cl2=Br2+2Cl-,该反应是单质与化合物反应产生新的单质和新的化合物,因此都属于置换反应,正确。
答案选C。

【题目】工业制备氮化硅的反应为:3SiCl4(g)+2N2(g)+6H2(g)![]() Si3N4(s)+12HCl(g) ΔH<0,将0.3 molSiCl4 和一定量 N2、H2 投入2 L反应容器,只改变温度条件测得Si3N4的质量变化如下表:
Si3N4(s)+12HCl(g) ΔH<0,将0.3 molSiCl4 和一定量 N2、H2 投入2 L反应容器,只改变温度条件测得Si3N4的质量变化如下表:
时间/min 质量/g 温 度/℃ | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
250 | 0.00 | 1.52 | 2.80 | 3.71 | 4.73 | 5.60 | 5.60 |
300 | 0.00 | 2.13 | 3.45 | 4.48 | 4.48 | 4.48 | 4.48 |
下列说法正确的是
A. 250℃,前 2min, Si3N4 的平均反应速率为 0.02 mol·L-1·min-1
B. 反应达到平衡时, 两种温度下 N2 和 H2 的转化率之比相同
C. 达到平衡前, 300℃条件的反应速率比 250℃快; 平衡后, 300℃比 250℃慢
D. 反应达到平衡时, 两种条件下反应放出的热量一样多