题目内容
8.在标准状况下,wL氮气含有x个N原子,用ω和x表示阿伏加德罗常数为( )| A. | wx mol-1 | B. | 22.4x mol-1 | C. | $\frac{22.4x}{ω}$mol-1 | D. | $\frac{11.2x}{ω}$mol-1 |
分析 标准状况下气体摩尔体积为22.4L/mol,根据n=$\frac{VL}{22.4L/mol}$计算出WL氮气的物质的量,再根据阿伏伽德罗常数的表达式NA=$\frac{N}{n}$进行计算即可.
解答 解:标准状况下,WL氮气的物质的量为:n(N2)=$\frac{ωL}{22.4L/mol}$=$\frac{ω}{22.4}$mol,则阿伏伽德罗常数为:NA=$\frac{N}{n}$=$\frac{\frac{x}{ω}}{22.4}$=$\frac{22.4x}{ω}$mol-1,故选C.
点评 本题考查阿伏加德罗常数的简单计算,题目难度不大,注意明确阿伏伽德罗常数的概念及计算方法,掌握好以物质的量、标况下的气体摩尔体积与阿伏加德罗常数的关系为解答本题的关键.

练习册系列答案
 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案
相关题目
19.天平的两个托盘上均放有盛200mL 0.5mol•L-1的H2SO4溶液的烧杯,天平平衡,向两烧杯中分别加入Na和Mg单质,反应完成后天平仍保持平衡,则加入的两金属可能组合是( )
| A. | 各加入2.3g | B. | 各加入0.1mol | C. | 各加入0.01mol | D. | 各加入0.23g |
16.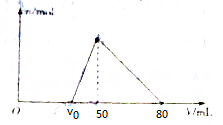 将一定量的Al2O3加入到100mL NaOH溶液中,固体全部溶解,向所得溶液中逐滴加入1.0mol•L-1的盐酸,所得沉淀的物质的量与加入盐酸体积的关系如图所示(不考虑溶液体积的变化),则下列说法正确的是( )
将一定量的Al2O3加入到100mL NaOH溶液中,固体全部溶解,向所得溶液中逐滴加入1.0mol•L-1的盐酸,所得沉淀的物质的量与加入盐酸体积的关系如图所示(不考虑溶液体积的变化),则下列说法正确的是( )
 将一定量的Al2O3加入到100mL NaOH溶液中,固体全部溶解,向所得溶液中逐滴加入1.0mol•L-1的盐酸,所得沉淀的物质的量与加入盐酸体积的关系如图所示(不考虑溶液体积的变化),则下列说法正确的是( )
将一定量的Al2O3加入到100mL NaOH溶液中,固体全部溶解,向所得溶液中逐滴加入1.0mol•L-1的盐酸,所得沉淀的物质的量与加入盐酸体积的关系如图所示(不考虑溶液体积的变化),则下列说法正确的是( )| A. | NaOH溶液的浓度为1.0mol•L-1 | |
| B. | Al2O3的质量为0.51g | |
| C. | v0的数值为35 | |
| D. | 沉淀量达到最大时,溶液中的溶质有两种 |
7.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | N2(g)+3H2(g)?2NH3(g)△H=-92.0 kJ•mol-1,吸收的能量为46.0 kJ,则形成N-H键的数目为3NA | |
| B. | 常温下,向一密闭容器中加入2molNO与1molO2,容器中的分子数目小于2NA | |
| C. | 18gD2O(2H2O)中,含有的中子总数为10NA | |
| D. | 1.0mol•L-1NaCl溶液中含有NA个Cl- |
4.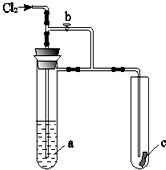 如图所示,将氯气通入装置.若打开活塞b,则小试管里的干燥品红试纸c不褪色;若关闭活塞b,则c不久褪色.则a溶液是( )
如图所示,将氯气通入装置.若打开活塞b,则小试管里的干燥品红试纸c不褪色;若关闭活塞b,则c不久褪色.则a溶液是( )
 如图所示,将氯气通入装置.若打开活塞b,则小试管里的干燥品红试纸c不褪色;若关闭活塞b,则c不久褪色.则a溶液是( )
如图所示,将氯气通入装置.若打开活塞b,则小试管里的干燥品红试纸c不褪色;若关闭活塞b,则c不久褪色.则a溶液是( )| A. | 浓盐酸 | B. | 浓硫酸 | C. | 饱和食盐水 | D. | NaOH溶液 |
2.下列有关项目的比较中,错误的是( )
| A. | 酸性:H2SO4>HClO4 | B. | 氧化性:Fe3+>Fe2+ | ||
| C. | 稳定性:HBr<HCl | D. | 原子半径 Na>Mg |
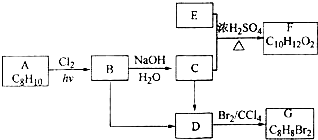
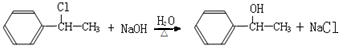 ;
;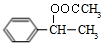 ;
;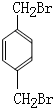 (填结构简式).
(填结构简式).